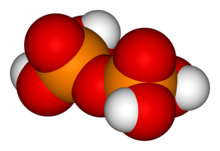
Kwas pirofosforowy - Pyrophosphoric acid

|
|
|
|
| Nazwy | |
|---|---|
|
Nazwy IUPAC
Kwas difosforowy
μ-oksydobis (dihydroksydoksydofosfor) |
|
| Inne nazwy
Kwas difosforowy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA |
100.017.795 |
|
PubChem CID
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| H 4 P 2 O 7 | |
| Masa cząsteczkowa | 177,97 g / mol |
| Temperatura topnienia | 71,5 ° C (160,7 ° F, 344,6 K) |
| Wyjątkowo rozpuszczalny | |
| Rozpuszczalność | Bardzo dobrze rozpuszczalny w alkoholu , eterze |
| Baza koniugatu | Pirofosforan |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Kwas pirofosforowy , znany również jako kwas difosforowy , jest związkiem nieorganicznym o wzorze H 4 P 2 O 7 lub, bardziej opisowo, [(HO) 2 P (O)] 2 O. Bezbarwny i bezwonny, rozpuszczalny w wodzie , eter dietylowy i alkohol etylowy . Bezwodny kwas krystalizuje w postaci dwóch polimorfów , które topią się w 54,3 ° C i 71,5 ° C. Związek nie jest szczególnie użyteczny, poza tym, że jest składnikiem kwasu polifosforowego i sprzężonego kwasu anionu pirofosforanowego. Aniony , sole i estry kwasu pirofosforowego nazywane są pirofosforanami .
Przygotowanie
Najlepiej przygotować go przez wymianę jonową z pirofosforanu sodu lub przez obróbkę pirofosforanu ołowiu siarkowodorem . Nie jest przygotowywany przez odwodnienie kwasu fosforowego. Zamiast tego kwas pirofosforowy jest produkowany jako jedyny z produktów.
Reakcje
Po stopieniu kwas pirofosforowy szybko tworzy równowagową mieszaninę kwasu fosforowego, pirofosforowego i polikwasów fosforowych. Procent wagowy kwasu pirofosforowego wynosi około 40% i jego rekrystalizacja ze stopu jest trudna. W roztworze wodnym kwas pirofosforowy, podobnie jak wszystkie kwasy polifosforowe, hydrolizuje i ostatecznie ustala się równowaga między kwasem fosforowym, kwasem pirofosforowym i kwasami polifosforowymi.
- H 4 P 2 O 7 + H 2 O ⇌ 2H 3 PO 4
Kwas pirofosforowy jest średnio mocnym kwasem nieorganicznym .
Bezpieczeństwo
Chociaż kwas pirofosporowy jest żrący, nie wiadomo, czy jest toksyczny w inny sposób.
Historia
Nazwa kwas pirofosforowy została nadana przez „pana Clarke'a z Glasgow” w 1827 r., Któremu przypisuje się odkrycie po podgrzaniu do czerwonego ciepła soli sodowej fosforanu. Stwierdzono, że kwas fosforowy po podgrzaniu do czerwonego ciepła tworzy kwas pirofosforowy, który można łatwo przekształcić w kwas fosforowy za pomocą gorącej wody.
Zobacz też
- Pirofosforan sodu
- Choroba odkładania dwuwodnego pirofosforanu wapnia
- Pirofosforan dimetyloallilu
- ADP
- ATP
- Kwasy ortokwasy
- kwas trifosforowy
Bibliografia
- ^ Corbridge, D. (1995). „Rozdział 3: Fosforany”. Studia z chemii nieorganicznej vol. 20 . Elsevier Science BV s. 169–305. doi : 10.1016 / B978-0-444-89307-9.50008-8 . ISBN 0-444-89307-5 .
- ^ Karta charakterystyki materiału: MSDS kwasu pirofosforowego www.sciencelab.com
- ^ Beck, Lewis Caleb (1834). Podręcznik chemii: zawierający skondensowany pogląd na obecny stan nauki, z licznymi odniesieniami do bardziej obszernych traktatów, oryginalnych publikacji itp . EW & C Skinner. p. 160 . Źródło 30 stycznia 2015 r .
