trifluorometanosulfonian skandu(III) - Scandium(III) trifluoromethanesulfonate

|
|
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
trifluorometanosulfonian skandu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.157,499 |
|
Identyfikator klienta PubChem
|
|
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 3 F 9 O 9 S 3 Sc | |
| Masa cząsteczkowa | 492,16 g/mol |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | Karta charakterystyki dla Oksfordu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
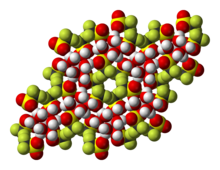
trifluorometanosulfonian skandu , powszechnie nazywany triflatem skandu , jest związkiem chemicznym o wzorze Sc(SO 3 CF 3 ) 3 , solą składającą się z kationów skandu Sc 3+ i triflatu SO
3CF−
3 aniony .
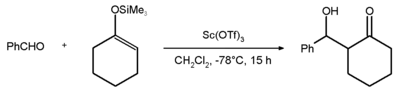
Triflat skandu jest używany jako odczynnik w chemii organicznej jako kwas Lewisa . W porównaniu z innymi kwasami Lewisa, odczynnik ten jest stabilny w stosunku do wody i często może być stosowany w reakcjach organicznych jako prawdziwy katalizator, a nie stosowany w ilościach stechiometrycznych. Związek wytwarza się w reakcji tlenku skandu z kwasem trifluorometanosulfonowym .
Przykładem zastosowań naukowych trifluorometanosulfonianu skandu jest addycja aldolowa Mukaiyama reakcja pomiędzy benzaldehydem a sililowy eter enolu z cykloheksanonem z 81% wydajnością .