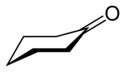
Cykloheksanon - Cyclohexanone
|
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Cykloheksanon |
|||
| Inne nazwy
oksocykloheksan, keton pimelinowy, ketoheksametylen, keton cykloheksylowy, ketocykloheksan, heksanon, Hydrol-O, Sextone, K, Anone
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Karta informacyjna ECHA |
100.003.302 |
||
| Numer WE | |||
| KEGG | |||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 6 H 10 O | |||
| Masa cząsteczkowa | 98,15 g/mol | ||
| Wygląd | Bezbarwna ciecz | ||
| Zapach | miętowy lub aceton -jak | ||
| Gęstość | 0,9478 g/ml, ciecz | ||
| Temperatura topnienia | -47 ° C (-53 ° F; 226 K) | ||
| Temperatura wrzenia | 155,65 ° C (312,17 ° F; 428,80 K) | ||
| 8,6 g/100 ml (20 °C) | |||
| Rozpuszczalność we wszystkich rozpuszczalnikach organicznych | Mieszalny | ||
| Ciśnienie pary | 5 mmHg (20°C) | ||
| -62,04 x 10 -6 cm 3 / mol | |||
|
Współczynnik załamania ( n D )
|
1.447 | ||
| Lepkość | 2,02 cP w 25 °C | ||
| Termochemia | |||
|
Standardowa
entropia molowa ( S |
+229,03 JK -1 .mol -1 | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
−270,7 kJ mol −1 | ||
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
-3519.3 kJmol -1 | ||
| Zagrożenia | |||
| Piktogramy GHS |
  
|
||
| Hasło ostrzegawcze GHS | Niebezpieczeństwo | ||
| H226 , H302 , H312 , H332 , H315 , H318 | |||
| P280 , P305+351+338 | |||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | 44 ° C (111 ° F; 317 K) | ||
| 420 ° C (788 ° F; 693 K) | |||
| Granice wybuchowości | 1,1-9,4% | ||
| Dawka lub stężenie śmiertelne (LD, LC): | |||
|
LC 50 ( mediana stężenia )
|
8000 ppm (szczur, 4 godz.) | ||
|
LC Lo ( najniższa opublikowana )
|
4706 ppm (mysz, 1,5 godz.) | ||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
TWA 50 ppm (200 mg/m 3 ) | ||
|
REL (zalecane)
|
TWA 25 ppm (100 mg/m 3 ) [skóra] | ||
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
700 ppm | ||
| Związki pokrewne | |||
|
Powiązane ketony
|
Cyklopentanon , cykloheptanon | ||
|
Związki pokrewne
|
Cykloheksanol | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Cykloheksanon jest związkiem organicznym o wzorze (CH 2 ) 5 CO. Cząsteczka składa się z sześciowęglowej cyklicznej cząsteczki z ketonową grupą funkcyjną. Ten bezbarwny olej ma zapach przypominający zapach acetonu . Z biegiem czasu próbki cykloheksanonu przybierają żółty kolor. Cykloheksanon jest słabo rozpuszczalny w wodzie i miesza się z powszechnymi rozpuszczalnikami organicznymi. Miliardy kilogramów są produkowane rocznie, głównie jako prekursor nylonu .
Produkcja
Cykloheksanon jest wytwarzany przez utlenianie cykloheksanu w powietrzu, zwykle przy użyciu katalizatorów kobaltowych:
- C 6 H 12 + O 2 → (CH 2 ) 5 CO + H 2 O
W procesie tym współtworzy się cykloheksanol , a ta mieszanina, zwana „olejem KA” dla oleju ketonowo-alkoholowego, jest głównym surowcem do produkcji kwasu adypinowego . Utlenianie obejmuje rodniki i pośrednictwo w wodoronadtlenku C 6 H 11 O 2 H W niektórych przypadkach, oczyszczonego cykloheksanol, otrzymanego przez uwodnienie cykloheksen jest prekursorem. Alternatywnie, cykloheksanon można wytworzyć w wyniku częściowego uwodorniania z fenolem :
- C 6 H 5 OH + 2 H 2 → (CH 2 ) 5 CO
Proces ten można również dostosować tak, aby sprzyjał tworzeniu się cykloheksanolu.
ExxonMobil opracował proces hydroalkilowania benzenu do cykloheksylobenzenu . Ten ostatni produkt jest utleniany do wodoronadtlenku, a następnie rozszczepiany do fenolu i cykloheksanonu. Dlatego ten nowszy proces bez wytwarzania produktu ubocznego acetonu wydaje się atrakcyjny i jest podobny do procesu kumenu, ponieważ wodoronadtlenek tworzy się, a następnie rozkłada, dając dwa kluczowe produkty.
Metody laboratoryjne
Cykloheksanon można otrzymać z cykloheksanolu przez utlenianie tritlenkiem chromu ( utlenianie Jonesa ). Alternatywna metoda wykorzystuje bezpieczniejszy i łatwiej dostępny utleniacz podchloryn sodu .
Zastosowania
Zdecydowana większość cykloheksanonu jest zużywana w produkcji prekursorów Nylonu 6,6 i Nylonu 6 . Około połowa światowych dostaw jest przetwarzana na kwas adypinowy , jeden z dwóch prekursorów nylonu 6,6 . W tym zastosowaniu olej KA (patrz wyżej) jest utleniany kwasem azotowym . Druga połowa dostarczanego cykloheksanonu jest przekształcana w oksym cykloheksanonu . W obecności katalizatora kwasu siarkowego oksym przekształca się w kaprolaktam , prekursor nylonu 6 :
Reakcje laboratoryjne
Oprócz reakcji na dużą skalę prowadzonych w przemyśle polimerów, opracowano wiele reakcji dla cykloheksanonu. W obecności światła ulega alfa-chlorowaniu dając 2-chlorocykloheksanon. Tworzy eter trimetylosililenolu po potraktowaniu chlorkiem trimetylosililu w obecności zasady. Tworzy również enaminę z pirolidyną.
Niedozwolone użycie
Cykloheksanon był używany do nielegalnej produkcji fencyklidyny i jej analogów i jako taki jest często poddawany dodatkowym kontrolom przed zakupem.
Bezpieczeństwo
Podobnie jak cykloheksanol , cykloheksanon nie jest rakotwórczy i jest umiarkowanie toksyczny, przy TLV wynoszącym 25 ppm dla oparów. To jest drażniące.
Bibliografia
- ^ Międzynarodowa Karta Bezpieczeństwa Chemicznego 0425
- ^ Kieszonkowy przewodnik po zagrożeniach chemicznych NIOSH
- ^ a b c d Kieszonkowy przewodnik po zagrożeniach chemicznych NIOSH. „#0166” . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ Wyciąg danych z Landolt-Börnstein IV/25: Lepkość czystych płynów organicznych i binarnych mieszanin płynów
- ^ Sigma-Aldrich - Cykloheksanon
- ^ B C, Sigma-Aldrich Co. , cykloheksanonu . Pobrano 20.11.2017.
- ^ a b „Cykloheksanon” . Stężenia bezpośrednio niebezpieczne dla życia lub zdrowia (IDLH) . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ B c d e Michael T. Musser "cykloheksanolu i cykloheksanonu" w Ullmanns Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi : 10,1002 / 14356007.a08_217
- ^ Plotkin, Jeffrey S. (21.03.2016). „Co nowego w produkcji fenolu?” . Amerykańskie Towarzystwo Chemiczne. Zarchiwizowane od oryginału dnia 2019-10-27 . Źródło 2019-10-27 .
- ^ „Fenol - Niezbędny przemysł chemiczny w Internecie” . 2017-01-11 . Źródło 2019-10-27 .
- ^ „Zarchiwizowana kopia” . Zarchiwizowane od oryginału w dniu 2012-04-26 . Źródło 09.07.2012 .CS1 maint: zarchiwizowana kopia jako tytuł ( link )
- ^ MS Newman, MD Farbman, H. Hipsher (1945). „2-chlorocykloheksanon”. Organizacja Syntezator . 25 : 22. doi : 10.15227/orgsyn.025.0022 .CS1 maint: używa parametru autorów ( link )
- ^ Valsamma Varghese, Manasi Saha, Kenneth M. Nicholas (1989). „Alkilacje przy użyciu soli heksakarbonylo (propargilium) dikobaltu: 2-(1-metylo-2-propynylo) cykloheksanon”. Organizacja Syntezator . 67 : 141. doi : 10.15227/orgsyn.067.0141 .CS1 maint: używa parametru autorów ( link )
- ^ RB Woodward , IJ Pachter, ML Scheinbaum (1974). „2,2-(trimetylenoditio)cykloheksanon”. Organizacja Syntezator . 54 : 39. doi : 10.15227/orgsyn.054.0039 .CS1 maint: używa parametru autorów ( link )
- ^ Shulgin, AT; MacLean, DE (25 września 2008 r.). „Nielegalna synteza fencyklidyny (PCP) i kilka jej analogów”. Toksykologia kliniczna . 9 (4): 553–560. doi : 10.3109/15563657608988157 .