Czterofluorek siarki - Sulfur tetrafluoride

|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Nazwa IUPAC
Fluorek siarki (IV)
|
|||
| Inne nazwy
Czterofluorek siarki
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.029.103 |
||
|
PubChem CID
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 2418 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| SF 4 | |||
| Masa cząsteczkowa | 108,07 g / mol | ||
| Wygląd | bezbarwny gaz | ||
| Gęstość | 1,95 g / cm 3 , -78 ° C, | ||
| Temperatura topnienia | -121,0 ° C | ||
| Temperatura wrzenia | -38 ° C | ||
| reaguje | |||
| Ciśnienie pary | 10,5 atm (22 ° C) | ||
| Struktura | |||
| Huśtawka ( C 2 v ) | |||
| 0,632 D | |||
| Zagrożenia | |||
| Główne zagrożenia | wysoce toksyczny żrący |
||
| Arkusz danych dotyczących bezpieczeństwa | ICSC 1456 | ||
| NFPA 704 (ognisty diament) | |||
| NIOSH (limity narażenia zdrowotnego w USA): | |||
|
PEL (dopuszczalny)
|
Żaden | ||
|
REL (zalecane)
|
C 0,1 ppm (0,4 mg / m 3 ) | ||
|
IDLH (bezpośrednie zagrożenie)
|
ND | ||
| Związki pokrewne | |||
|
Inne aniony
|
Dichlorek siarki Dibromek siarki Trifluorek siarki |
||
|
Inne kationy
|
Difluorek tlenu Tetrafluorek selenu Tetrafluorek telluru |
||
|
Powiązane fluorki siarki
|
Dwufluorek siarki Dwufluorek siarki Dekafluorek siarki Sześciofluorek siarki |
||
|
Związki pokrewne
|
Fluorek tionylu | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencje Infobox | |||
Czterofluorek siarki to związek chemiczny o wzorze S F 4 . Jest to bezbarwny, korozyjny gaz, który uwalnia niebezpieczny HF pod wpływem wody lub wilgoci. Pomimo tych niepożądanych właściwości, związek ten jest użytecznym odczynnikiem do wytwarzania związków fluoroorganicznych , z których niektóre są ważne w przemyśle farmaceutycznym i chemicznym .
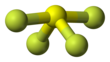
Struktura
Siarka w SF 4 jest na formalnym stopniu utlenienia +4 . Z całkowitej liczby sześciu elektronów walencyjnych siarki dwa tworzą samotną parę . Strukturę SF 4 można zatem przewidzieć, stosując zasady teorii VSEPR : jest to kształt huśtawki z literą S w środku. Jedna z trzech pozycji równikowych jest zajęta przez niezwiązaną samotną parę elektronów. W konsekwencji cząsteczka ma dwa różne typy ligandów F, dwa osiowe i dwa równikowe . Odpowiednie odległości wiązania to S – F ax = 164,3 pm i S – F eq = 154,2 pm. Typowe jest, że osiowe ligandy w hiperwalentnych cząsteczkach są związane słabiej. W przeciwieństwie do SF 4 , pokrewna cząsteczka SF 6 ma siarkę w stanie 6+, żadne elektrony walencyjne nie pozostają niezwiązane z siarką, stąd cząsteczka przyjmuje wysoce symetryczną strukturę oktaedryczną. Co więcej, w przeciwieństwie do SF 4 , SF 6 jest wyjątkowo obojętny chemicznie.
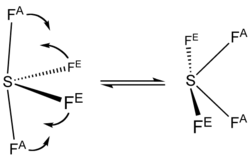
19 C -NMR widmo SF 4 pokazuje tylko jeden sygnał, który wskazuje, że osiowe i ekwatorialne pozycji atomem F szybko przekształcać się poprzez pseudorotation .
Synteza i produkcja
SF 4 powstaje w reakcji SCl 2 i NaF w acetonitrylu :
- 3 SCl 2 + 4 NaF → SF 4 + S 2 Cl 2 + 4 NaCl
SF 4 wytwarza się również w nieobecności rozpuszczalnika w podwyższonej temperaturze.
Alternatywnie SF 4 z wysoką wydajnością jest wytwarzany przy użyciu siarki (S) , NaF i chloru (Cl 2 ) bez medium reakcyjnego, również w mniej pożądanych podwyższonych temperaturach reakcji (np. 225–450 ° C).
Wykazano niskotemperaturową (np. 20–86 ° C) metodę wytwarzania SF 4 z wysoką wydajnością, bez konieczności stosowania medium reakcyjnego, wykorzystującą brom (Br 2 ) zamiast chloru (Cl 2 ) , S i KF :
- S + (2 + x ) Br 2 + 4 KF → SF 4 ↑ + x Br 2 + 4 KBr
Zastosowanie SF 4 do syntezy fluorowęglowodorów
W syntezie organicznej , SF 4 służy do konwersji COH i grupy C = O w CF CF 2 grupy, odpowiednio. Niektóre alkohole łatwo dają odpowiedni fluorowęglowodór . Ketony i aldehydy dają geminalne difluorki. Obecność protonów alfa dla karbonylu prowadzi do reakcji ubocznych i zmniejszenia (30–40%) wydajności. Ponadto diole mogą dać cykliczny siarczyn estry (RO) 2 SO. Kwasy karboksylowe przekształcają się w pochodne trifluorometylowe. Na przykład, traktowanie kwasu heptanowego z SF 4 w 100-130 ° C wytwarza 1,1,1 trifluoroheptane. Heksafluoro-2-butyn można podobnie wytwarzać z kwasu acetylenodikarboksylowego . Produkty uboczne tych fluorowania, w tym nieprzereagowany SF 4 razem z SOF 2 i SO 2 , są toksyczne, ale można je zneutralizować przez traktowanie ich wodnym KOH.
Zastosowanie SF 4 jest zastępowany w ostatnich latach bardziej dogodnie manipulowana trifluorku dietyloaminosiarki , Et 2 NSF 3 , „DAST”, gdzie Et = CH 3 CH 2 . Ten odczynnik jest przygotowany z SF 4 :
- SF 4 + Me 3 SiNEt 2 → Et 2 NSF 3 + Me 3 SiF
Inne reakcje
Pentafluorek chlorku siarki ( SF
5 Cl ), użyteczne źródło grupy SF 5 , przygotowuje się z SF 4 .
Hydroliza SF 4 daje dwutlenek siarki :
- SF 4 + 2 H 2 O → SO 2 + 4 HF
Reakcja ta przebiega poprzez pośrednictwo w tionylu fluorku , która zazwyczaj nie przeszkadza w wykorzystaniu SF 4 jako reagent.
Toksyczność
SF
4 reaguje w płucach z wilgocią, wytwarzając dwutlenek siarki i fluorowodór :
- SF 4 + 2 H 2 O → SO 2 + 4 HF