Zwitterion - Zwitterion
W chemii , A amfoteryczny ( / T e v ɪ t ə ˌ R aɪ ə n / TSVIT -ə żyto-ən , z niemieckiego Zwitter[ˈtsvɪtɐ] " hermafrodyta ", zwana także solą wewnętrzną , to cząsteczka zawierająca równą liczbę dodatnio i ujemnie naładowanych grup funkcyjnych . Na przykład w przypadku aminokwasów w roztworze zostanie ustalona równowaga chemiczna między cząsteczką „rodzicielską” a jonem obojnaczym.
Betainy są jonami obojnaczymi, które nie mogą izomeryzować do postaci całkowicie neutralnej, na przykład gdy ładunek dodatni znajduje się na czwartorzędowej grupie amonowej . Podobnie cząsteczka zawierająca grupę fosfoniową i grupę karboksylanową nie może ulegać izomeryzacji.
Aminokwasy

Równowagę ustala się w dwóch etapach. W jednym etapie proton jest przenoszony z grupy karboksylowej do cząsteczki wody.
-
h
2N(R)CO
2H + H
2O ⇌ H
2N(R)CO−
2+ H
3O+
W drugim etapie proton jest przenoszony z jonu hydroniowego do grupy aminowej
-
h
2N(R)CO−
2+ H
3O+
⇌ H
3n+
(R)CO−
2+ H
2O
Ogólnie reakcja jest reakcją izomeryzacji
-
h
2N(R)CO
2H ⇌ H
3n+
(R)CO−
2
Stosunek stężeń dwóch związków w roztworze jest niezależny od pH, ponieważ jest równy wartości stałej równowagi K dla reakcji izomeryzacji.
[X] oznacza stężenie związku chemicznego X w równowadze. Ogólnie przyjmuje się, że K > 1, to znaczy, że jon obojnaczy jest dominującym izomerem aminokwasu w roztworze wodnym. Na podstawie analizy teoretycznej zasugerowano, że jon obojnaczy jest stabilizowany w roztworze wodnym przez wiązanie wodorowe z cząsteczkami rozpuszczalnika i wody. Analiza danych dyfrakcji neutronów dla glicyny wykazała, że w stanie stałym była ona w postaci obojnaczej i potwierdziła obecność wiązań wodorowych. Obliczenia teoretyczne zostały wykorzystane do wykazania, że jony obojnacze mogą być również obecne w fazie gazowej w niektórych przypadkach innych niż proste przeniesienie kwasu karboksylowego do aminy.
P K A wartości dla odprotonowania powszechnych aminokwasów obejmują przybliżony zakres2,15 ± 0,2 . Jest to również zgodne z tym, że jon obojnaczy jest dominującym izomerem obecnym w roztworze wodnym. Dla porównania prosty kwas karboksylowy kwas propionowy ( CH
3CH
2WSPÓŁ
2H ) ma ap K o wartości 4,88.
Inne związki
Izomery kwasu amidosulfonowego z jonem obojnaczym (po prawej)
Struktura H 4 EDTA
Kwas amidosulfonowy krystalizuje w postaci jonu dwubiegunowego.
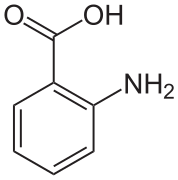
W kryształach kwasu antranilowego w komórce elementarnej znajdują się dwie cząsteczki . Jedna cząsteczka jest w postaci jonu obojnaczego, druga nie.
W postaci stałej, H 4 EDTA jest amfoteryczny dwa protony zostały przekazane z grup karboksylowych do atomów azotu.
Studia teoretyczne
Chociaż równowaga w roztworze między związkiem a jego izomerem obojnaczym nie może być badana doświadczalnie, pewien wgląd można uzyskać na podstawie wyników obliczeń teoretycznych. Dobrym przykładem jest z fosforanu pirydoksalu, formy witaminy B 6 . Przewidywano uzyskanie równowagi tautomerycznej w wodnym roztworze tego związku, faworyzując jon obojnaczy, w którym proton jest przenoszony z fenolowej grupy -OH na atom azotu.
Betainy i podobne związki
Związek trimetyloglicyny , który został wyizolowany z buraka cukrowego , został nazwany „betainą”. Później odkryto inne związki, które zawierają ten sam motyw strukturalny, czwartorzędowy atom azotu z dołączoną do niego grupą karboksylanową poprzez łącznik –CH 2 – . W chwili obecnej wszystkie związki, których struktura zawiera ten motyw, znane są jako betainy. Betainy nie ulegają izomeryzacji, ponieważ grupy chemiczne przyłączone do atomu azotu nie są labilne . Związki te można sklasyfikować jako trwałe jony obojnacze, ponieważ izomeryzacja do cząsteczki bez ładunków elektrycznych nie zachodzi lub jest bardzo powolna.
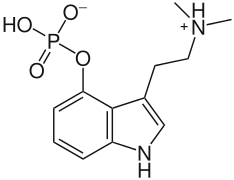
Inne przykłady trwałych jonów obojnaczych obejmują fosfatydylocholiny i psilocybinę , które również zawierają czwartorzędowy atom azotu, ale z ujemnie naładowaną grupą fosforanową zamiast grupy karboksylanowej; oraz płucne środki powierzchniowo czynne, takie jak dipalmitoilofosfatydylocholina .
Trimetyloglicyna (nazwa zwyczajowa betaina)
Przykład fosfatydylocholiny
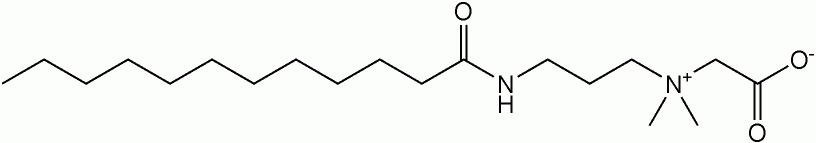
Lauramidopropyl betaina, główny składnik kokamidopropylobetainy
Sprzężone Zwitterions
Silnie spolaryzowane związki sprzężone (sprzężone jony dwubiegunowe) są zazwyczaj bardzo reaktywne, mają charakter dwurodnikowy , aktywują silne wiązania i małe cząsteczki oraz służą jako przejściowe związki pośrednie w katalizie. Jednostki donora-akceptora mają szerokie zastosowanie w fotochemii ( fotoindukowany transfer elektronów ), elektronice organicznej , przełączaniu i wykrywaniu .

![{\ Displaystyle K = \ operatorname {\ Frac {[H_ {3}N ^ {+} (R) CO_ {2} ^ {-}] {[H_ {2} N (R) CO_ {2} H] }} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/cb3b1f175dd0458c9c2643ed5f88241423250f16)