Monofluorek chloru - Chlorine monofluoride
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Monofluorek chloru
|
|
| Inne nazwy
Fluorek chloru
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.029.300 |
|
PubChem CID
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| ClF | |
| Masa cząsteczkowa | 54,45 g / mol |
| Gęstość | 1,62 g ml (ciecz, −100 ° C) |
| Temperatura topnienia | -155,6 ° C (-248,1 ° F; 117,5 K) |
| Temperatura wrzenia | −100,1 ° C (−148,2 ° F; 173,1 K) |
| Struktura | |
| 0,881 D (2,94 x 10 -30 C, m) |
|
| Termochemia | |
|
Pojemność cieplna ( C )
|
33,01 JK −1 mol −1 |
|
Entropia trzonowa standardowa ( S |
217,91 JK −1 mol −1 |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
−56,5 kJ mol −1 |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
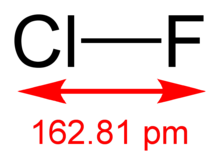
Monofluorek chloru to lotny związek międzyhalogenowy o wzorze chemicznym ClF. W temperaturze pokojowej jest bezbarwnym gazem i jest stabilny nawet w wysokich temperaturach. Po schłodzeniu do -100 ° C, ClF skrapla się w postaci bladożółtej cieczy. Wiele z jego właściwości jest pośrednich między rodzicielskimi halogenami , Cl 2 i F 2 .
Reaktywność
Monofluorek chloru jest wszechstronnym środkiem fluorującym , który przekształca metale i niemetale w ich fluorki i uwalnia Cl 2 w procesie. Na przykład przekształca wolfram w sześciofluorek wolframu i selen w czterofluorek selenu :
- W + 6 ClF → WF 6 + 3 Cl 2
- Se + 4 ClF → SeF 4 + 2 Cl 2
FCI może również chlorofluorować związki, albo przez dodanie poprzez wiązanie wielokrotne lub przez utlenianie . Na przykład dodaje fluoru i chloru do węgla w tlenku węgla , uzyskując fluorek chlorku karbonylu:
