Pikolinian chromu(III) - Chromium(III) picolinate
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Nazwa IUPAC
Tris(pikolinian)chrom(III)
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.131.423 |
||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| Cr (C 6 H 4 NR 2 ), 3 | |||
| Masa cząsteczkowa | 418,33 g/mol | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Pikolinian chromu(III) (CrPic 3 ) to związek chemiczny sprzedawany jako suplement diety do leczenia cukrzycy typu 2 i promowania utraty wagi. Ten jasnoczerwony związek koordynacyjny jest pochodną chromu (III) i kwasu pikolinowego . W normalnym stanie zdrowia do wykorzystania glukozy przez insulinę potrzebne są duże ilości chromu , ale niedobór jest niezwykle powszechny i zaobserwowano go u osób otrzymujących dożylnie 100% swoich potrzeb żywieniowych , tj . stosując całkowitą dietę żywieniową pozajelitową . Chrom został zidentyfikowany jako regulujący insulinę poprzez zwiększenie wrażliwości receptora insulinowego . Jako taki, pikolinian chromu(III) został zaproponowany do leczenia cukrzycy typu 2 , chociaż jego skuteczność pozostaje kontrowersyjna ze względu na sprzeczne dowody z badań na ludziach.
Historia
Badanie z 1989 r. sugerowało, że pikolinian chromu(III) może wspomagać utratę wagi i zwiększać masę mięśniową, co doprowadziło do wzrostu stosowania suplementów z pikolinianem chromu(III) , co spowodowało, że przez pewien czas był on drugim najczęściej stosowanym suplementem za wapń. W przeglądzie Cochrane z 2013 r. nie udało się znaleźć „wiarygodnych dowodów do podejmowania decyzji firm” na poparcie takich twierdzeń. Badania ogólnie wykazały, że poprawia wrażliwość na insulinę, przedłużając jej aktywność lub zwiększając produkcję mRNA w celu wytworzenia większej liczby receptorów insuliny .
Wśród metali przejściowych , Cr 3+ jest najbardziej kontrowersyjna pod względem wartości odżywczej i toksyczności. Ta kontrowersja koncentruje się na tym, czy Cr 3+ zapewnia jakiekolwiek korzyści odżywcze. Co więcej, tę kontrowersję potęguje fakt, że nie scharakteryzowano struktury ani sposobu działania żadnych biocząsteczek zawierających Cr. Pierwszy eksperyment, który doprowadził do odkrycia Cr 3+ odgrywającego rolę w metabolizmie glukozy, sugerował, że biologicznie aktywna forma metalu występuje w białku zwanym czynnikiem tolerancji glukozy , jednak nowe dowody sugerują, że jest to po prostu artefakt uzyskany z izolacji. procedury. Jedynym akceptowanym wskaźnikiem niedoboru chromu jest odwrócenie objawów, które następuje po podawaniu suplementacji chromem(III) osobom całkowicie żywionym pozajelitowo .
Właściwości fizykochemiczne
Pikolinian chromu(III) jest różowo-czerwonym związkiem i po raz pierwszy opisano go w 1917 roku. Jest słabo rozpuszczalny w wodzie, a jego rozpuszczalność wynosi 600 μM w wodzie przy pH zbliżonym do obojętnego . Podobnie jak inne związki chromu(III), jest stosunkowo obojętny i niereaktywny, co oznacza, że kompleks ten jest stabilny w warunkach otoczenia, a do rozkładu związku wymagane są wysokie temperatury . Przy niższych poziomach pH kompleks hydrolizuje, uwalniając kwas pikolinowy i wolny Cr3+ .
Struktura
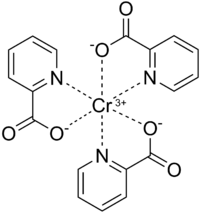
Pikolinian chromu(III) ma zniekształconą geometrię oktaedryczną i jest izostrukturalny z odpowiednikami kobaltu (III) i manganu (III). Chrom(III) jest twardym kwasem Lewisa i jako taki ma wysokie powinowactwo do tlenu karboksylowego i średnie powinowactwo pikolinianu do azotu pirydynowego . Każdy ligand pikolinianowy działa jako dwukleszczowy czynnik chelatujący i neutralizuje ładunek +3 Cr 3+ . Dowód na to, że współrzędne centrum Cr 3+ z azotem pirydynowym pochodzi z przesunięcia widma IR drgań C=N przy 1602,4 cm- 1 dla wolnego kwasu pikolinowego do 1565,9 cm- 1 dla pikolinianu chromu(III). Długość wiązania pomiędzy Kr 3+ i atomem azotu w pierścieniu pirydyny w zakresie picoliante od 2.047 do 2,048 nm . Ligand pikolinianowy współrzędne do Cr 3+ tylko po deprotonowaniu, co jest widoczne poprzez zanik pasm IR w zakresie od 2400-2800 cm- 1 (wyśrodkowany na 2500 cm- 1 ) i 1443 cm- 1 , odpowiadających rozciąganiu i zginaniu OH odpowiednio na karboksylowej grupie funkcyjnej. Co więcej, to przesunięcie IR wskazuje również, że tylko jeden atom tlenu z karboksylanu pikolinianu jest współrzędny do centrum Cr3+ . Długość wiązania Cr-O wynosi od 1,949 do 1,957 Å . Struktura krystaliczna została dopiero niedawno opisana w 2013 roku. Woda nie koordynuje się z centrum Cr 3+ i zamiast tego uważa się, że tworzy wiązanie wodorowe między innymi kompleksami Cr(Pic) 3 , tworząc sieć kompleksów Cr(Pic) 3 .
Biochemia pikolinianu chromu(III)
Chrom został zidentyfikowany jako niezbędny składnik odżywczy w utrzymaniu prawidłowego poziomu glukozy we krwi i jako taki proponuje się interakcję z dwiema naturalnie występującymi cząsteczkami znajdującymi się w organizmie. Te interakcje najprawdopodobniej zachodzą przez koordynację z twardymi ligandami, takimi jak asparaginian i glutaminian, ponieważ sam Cr(III) jest metalem twardym.
Wchłanianie i wydalanie pikolinianu chromu(III)
Po spożyciu pikolinianu chromu(III) i dostaniu się do żołądka następuje hydroliza kwasowa kompleksu w kontakcie z błoną śluzową żołądka . Zhydrolizowany Cr 3+ występuje w postaci heksaaqua i po osiągnięciu zasadowego pH jelita cienkiego polimeryzuje do nierozpuszczalnego wodorotlenku Cr(III) (proces olacji ) . Około 2% Cr 3+ jest wchłaniane przez jelita w postaci pikolinianu chromu(III) poprzez nienasycony transport bierny . Chociaż absorpcja jest niska, CrPic 3 pochłania skuteczniej niż inne źródła organiczne i nieorganiczne (tj. CrCl 3 i nikotynian chromu), a zatem gromadzi się w wyższych stężeniach w tkankach. Jest to jeden z głównych punktów sprzedaży pikolinianu chromu(III) w porównaniu z innymi suplementami chromu(III). Źródła organiczne mają tendencję do lepszej absorpcji, ponieważ zawierają ligandy, które są bardziej lipofilowe i zwykle neutralizują ładunek metalu, umożliwiając w ten sposób łatwiejsze przejście przez błonę jelitową.
Wykazano również, że czynniki dietetyczne wpływają na wchłanianie Cr 3+ . Skrobia , cukry proste , kwas szczawiowy i niektóre aminokwasy mają tendencję do zwiększania szybkości wchłaniania chromu(III). Jest to wynikiem chelatacji ligandów, przekształcającej hexaaqua Cr 3+ w bardziej lipofilowe formy. Natomiast wapń, magnez, tytan, cynk, wanad i żelazo zmniejszają szybkość wchłaniania. Przypuszczalnie jony te wprowadzają nową równowagę metal-ligand, zmniejszając w ten sposób pulę lipofilowych ligandów dostępnych dla Cr3+ . Po wchłonięciu do krwioobiegu 80% Cr 3+ z CrPic 3 przechodzi do transferyny. Dokładny mechanizm uwalniania jest obecnie znane, jednak uważa się, że nie występuje w pojedynczej redukcji elektronów, tak jak w przypadku Fe 3+ , ze względu na duży stopień nietrwałości Cr 2+ . Podany Cr 3+ można znaleźć we wszystkich tkankach w zakresie 10–100 μg/kg masy ciała. Jest wydalany głównie z moczem (80%), podczas gdy reszta jest wydalana z potem i kałem.
Wiązanie chromu(III) z transferyną
Transferyna , oprócz chromoduliny , została zidentyfikowana jako główny fizjologiczny środek transportu chromu, chociaż ostatnie badania wykazały, że Cr3+ w rzeczywistości uniemożliwia transferynie działanie jako środek transportu jonów metali. Chociaż transferyna jest wysoce specyficzna dla jonów żelazowych, w normalnych warunkach tylko 30% cząsteczek transferyny jest nasyconych jonami żelazowymi, co pozwala na wiązanie również innych metali, szczególnie tych o dużym stosunku ładunku do wielkości. Miejsca wiążące składają się z płata C i płata N, które mają prawie identyczną strukturę. Każdy płat zawiera kwas asparaginowy , histydynę , 2 reszty tyrozyny i jon wodorowęglanowy , który działa jak dwukleszczowy ligand umożliwiający wiązanie żelaza lub innych metali z transferyną w zniekształconej geometrii oktaedrycznej . Dowody potwierdzające wiązanie Cr3+ z transferyną pochodzą z rozległych badań klinicznych, które wykazały dodatnią korelację między poziomem ferrytyny a poziomem glukozy na czczo , insuliny i hemoglobiny glikowanej (Hb1Ac). Co więcej, badanie in vivo na szczurach wykazało, że 80% znakowanego izotopowo Cr3+ trafiło na transferynę, podczas gdy reszta była związana z albuminą . Badanie in vitro wykazało, że gdy chlorek chromu(III) został dodany do wyizolowanej transferyny, Cr3+ łatwo wiązał transferynę, ze względu na zmiany w widmie UV-Vis. Stałe tworzenie Cr 3+ w płacie C-10 to 1,41 x 10 M -1 i 2,04 x 10 5 M -1 do N-płata, co wskazuje, że Cr 3+ preferencyjnie wiąże się z C-płata. Ogólnie rzecz biorąc, stała tworzenia dla chromu(III) jest niższa niż dla jonów żelaza. Ligand wodorowęglanowy ma kluczowe znaczenie w wiązaniu Cr 3+, ponieważ gdy stężenia wodorowęglanów są bardzo niskie, powinowactwo wiązania jest również znacznie niższe. Badania elektronowego rezonansu paramagnetycznego (EPR) wykazały, że poniżej pH 6 chrom (III) wiąże się tylko z płatem N, a przy pH zbliżonym do obojętnego chrom (III) wiąże się również z płatem C. Chrom(III) może konkurować z jonem żelaza o wiązanie z płatem C, gdy nasycenie znacznie przekracza 30%. Jako takie, efekty te są obserwowane tylko u pacjentów cierpiących na hemochromatozę , chorobę magazynowania żelaza charakteryzującą się nadmiernym wysyceniem żelaza w transferynie.
Mechanizm akcji
Substancja wiążąca chrom o niskiej masie cząsteczkowej (LMWCr; znana również jako chromodulina) to oligopeptyd, który wydaje się wiązać chrom(III) w organizmie. Składa się z czterech reszt aminokwasowych; asparaginian , cysteina , glutaminian i glicyna , połączone czterema centrami ( Cr3+ ). Oddziałuje z receptorem insuliny, przedłużając aktywność kinazy poprzez stymulację szlaku kinazy tyrozynowej, prowadząc w ten sposób do poprawy wchłaniania glukozy. Mylona jest z czynnikiem tolerancji glukozy . Pomimo ostatnich prób scharakteryzowania chromoduliny, dokładna struktura jest wciąż stosunkowo nieznana.
Chociaż dokładny mechanizm działania chromoduliny na receptor insuliny jest obecnie nieznany, poniżej przedstawiono jeden powszechnie opisany mechanizm. Ten proponowany mechanizm ma największą zgodność z różnymi eksperymentami z udziałem chromoduliny.
Zwykle chromodulina występuje w postaci apochromoduliny, która jest wolna od jonów Cr(III) i ma minimalną aktywność na receptory insuliny. Apochromodulina jest przechowywana w jądrze komórkowym w komórkach wrażliwych na insulinę. Kiedy poziom glukozy we krwi wzrasta, insulina jest uwalniana do krwiobiegu i wiąże się z zewnętrzną podjednostką α receptora insuliny, białkiem transbłonowym . Receptor insuliny składa się z 2 zewnątrzkomórkowych podjednostek α i 2 transbłonowych podjednostek β. Gdy tylko insulina zwiąże się z receptorem insuliny, następuje konformacyjna zmiana receptora, powodująca fosforylację wszystkich 3 reszt tyrozyny (zlokalizowanych w podjednostkach β). To aktywuje receptor i pozwala mu przekazywać sygnał z insuliny do komórki. Jak wspomniano powyżej, zaabsorbowany pikolinian chromu(III) ostatecznie oddaje Cr3+ do transferyny. Z kolei transferyna transportuje Cr3+ do komórek wrażliwych na insulinę (tj. adipocytów ), gdzie wiąże się z apochromoduliną, tworząc holochromodulinę. Holochromodulina wiąże się z receptorem insuliny, co pomaga w utrzymaniu aktywnej konformacji receptora insuliny poprzez wydłużenie aktywności kinaz kinaz lub zwiększenie poziomu mRNA receptora insuliny , a tym samym obniżenie poziomu glukozy we krwi.
Eksperymenty były w stanie wykazać, że chrom (III) może się regulacji insuliny stymulowanego insuliną transdukcji sygnału poprzez wpływ na dalszych cząsteczek IR, o czym świadczy zwiększenie poziomu fosforylacji tyrozyny IRS-1 , podwyższony Thr308 i Ser473 fosforylacji z Akt i zwiększona aktywność PI3-K w różnych modelach komórkowych i zwierzęcych. Zwiększona fosforylacja IRS-1 doprowadziła do zwiększonej wrażliwości receptora insulinowego, podczas gdy Akt i PI3-K doprowadziły do zwiększonej translokacji GLUT4 na powierzchnię komórki, powodując w ten sposób większy wychwyt glukozy.
Wykazano również, że chrom(III) może łagodzić insulinooporność poprzez zmniejszenie stresu retikulum endoplazmatycznego (ER). Stres ER definiuje się jako akumulację nieprawidłowo sfałdowanych i niezwiniętych białek w świetle ER. Stres ER prowadzi do stymulacji kinazy końcowej c-Jun ( JNK ), która z kolei fosforyluje resztę seryny IRS, prowadząc do zahamowania kaskady sygnalizacji insuliny i mniejszego wychwytu glukozy. Wyniki eksperymentów sugerują, że chrom hamuje stres ER, a zatem tłumienie sygnalizacji insuliny jest wzmocnione. Dokładny mechanizm jest nieznany.
Innym sposobem, w jaki Cr(III) może przedłużyć aktywność kinazy receptora insuliny, jest utlenianie krytycznego miejsca aktywnego reszty cysteinowej na białkowej fosfatazie tyrozynowej 1B ( PTP1B ). Zwykle PTP1B defosforyluje reszty fosfotyrozyny, przeprowadzając atak nukleofilowy na grupę fosforanową poprzez jej resztę cysteinową, inaktywując w ten sposób receptor insuliny. Proces ten usuwa grupę fosforanową z reszty tyrozyny, tworząc grupę Cys-S-PO 3 2- , która jest następnie hydrolizowana przez wodę w celu regeneracji reszty cysteiny, co pozwala na kolejną rundę działania. Badania wykazały, że chrom(III) może w rzeczywistości powodować nieodwracalne zahamowanie PTP1B. Uważa się, że Cr(III) jest przekształcany w Cr(VI) lub Cr(V) (poprzez działanie oksydoreduktaz ), które następnie utleniają grupę tiolową reszty cysteiny na PTP1B do kwasu sulfenowego , co w konsekwencji uniemożliwia mu atakowanie fosforanu grupa na fosfotyrozynie. Jest to jednak tylko prawdopodobny mechanizm i nie wykazano żadnych bezpośrednich dowodów na poparcie tej hipotezy. Gdy kaskada sygnału jest wyłączona, holochromodulina jest eliminowana z moczem, ponieważ stała tworzenia jest zbyt duża, aby bezpośrednio usunąć Cr(III). Dowody eksperymentalne wykazały, że utrata chromoduliny z komórek jest skorelowana ze wzrostem stężenia chromu w moczu po spożyciu pokarmu bogatego w węglowodany (tj. glukozy).
Oświadczenia zdrowotne i debaty
Masy ciała
Pikolinian chromu(III) został wprowadzony na rynek w Stanach Zjednoczonych jako środek wspomagający rozwój ciała sportowców i jako środek na odchudzanie . Recenzje wykazały brak wpływu na wzrost mięśni lub utratę tkanki tłuszczowej lub niewielką, ale statystycznie istotną utratę wagi o 1,1 kg (2,4 funta) w badaniach trwających dłużej niż 12 tygodni. Europejski Urząd Bezpieczeństwa Żywności przeglądu piśmiennictwa i stwierdziła, że nie było wystarczających dowodów na poparcie roszczenia.
Cukrzyca
Istnieją twierdzenia, że suplementacja chromu w postaci pikolinianu pomaga w zmniejszeniu insulinooporności i poprawie metabolizmu glukozy , szczególnie u diabetyków typu 2 , ale przeglądy nie wykazały związku między chromem i stężeniami glukozy lub insuliny u osób bez cukrzycy i niejednoznaczne wyniki u osób z cukrzycą. Autorzy drugiego przeglądu wspomnieli, że pikolinian chromu obniżył poziom HbA1c o 0,7% u pacjentów z cukrzycą typu 2. Zaobserwowali, że badania niskiej jakości dawały większe pozytywne wyniki niż badania wyższej jakości. W dwóch przeglądach stwierdzono, że pikolinian chromu(III) może być skuteczniejszy w obniżaniu poziomu glukozy we krwi w porównaniu z innymi suplementami diety zawierającymi chrom.
W 2005 r. amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła kwalifikowane oświadczenie zdrowotne dotyczące pikolinianu chromu jako suplementu diety w odniesieniu do insulinooporności i ryzyka cukrzycy typu 2. Każda firma, która chce złożyć takie oświadczenie, musi użyć dokładnego sformułowania: „Jedno małe badanie sugeruje, że pikolinian chromu może zmniejszać ryzyko insulinooporności, a zatem prawdopodobnie może zmniejszać ryzyko cukrzycy typu 2. FDA stwierdza jednak, że istnienie takiego związku między pikolinianem chromu a insulinoopornością lub cukrzycą typu 2 jest wysoce niepewne”. W ramach procesu rozpatrywania petycji FDA odrzuciła inne roszczenia dotyczące zmniejszenia nienormalnie podwyższonego poziomu cukru we krwi, ryzyka chorób sercowo-naczyniowych, ryzyka retinopatii lub ryzyka choroby nerek. W 2006 roku FDA dodała, że „związek między spożyciem pikolinianu chromu(III) a insulinoopornością jest wysoce niepewny”.
Zmienność studiów
Nie zaobserwowano zgodności wyników klinicznych dotyczących pikolinianu chromu(III) z odpowiednim leczeniem cukrzycy typu 2. Wynika to ze stopnia nietolerancji glukozy u pacjentów biorących udział w badaniach klinicznych. Nietolerancja glukozy jest gradientem, a na jej intensywność wpływa pochodzenie etniczne, stopień otyłości, wiek, rozmieszczenie tkanki tłuszczowej i wiele innych czynników. W niektórych badaniach podawano niskie dawki suplementu, jednak należy podać odpowiednią ilość pikolinianu chromu(III) przed zaobserwowaniem jakiegokolwiek znaczącego spadku poziomu glukozy ze względu na różne poziomy insulinooporności. Inną ważną kwestią, o której należy wspomnieć, jest to, że cukrzyca nie zawsze jest spowodowana nietolerancją glukozy. Jak wspomniano wcześniej, wykazano, że Cr(III) wpływa tylko na nietolerancję glukozy, a nie na poziom insuliny. Ponadto środowiska, w których przeprowadzono badania, nie były spójne. Poziom stresu, diety spożywane przez pacjentów i genetyka pacjentów były różne wśród badanych osób. Odnosi się to również do kontroli w różnych badaniach, w których osoby chore na cukrzycę były już leczone szeroką gamą leków przeciwcukrzycowych, które mogą zmniejszać wpływ chromu na wpływ na aktywność insuliny. To może wyjaśniać, dlaczego badania na zwierzętach mają tendencję do uzyskiwania bardziej pozytywnych wyników ze względu na fakt, że te zwierzęta z cukrzycą nie były leczone lekami przeciwcukrzycowymi w grupie kontrolnej. Ponadto, jak wspomniano w części dotyczącej wchłaniania i wydalania, dieta wpływa na wchłanianie/biodostępność pikolinianu chromu(III). Łącznie te różne czynniki przyczyniły się do zmienności badań.
Bezpieczeństwo i toksyczność
Pojawiły się wstępne obawy, że pikolinian chromu(III) z większym prawdopodobieństwem powoduje uszkodzenie DNA i mutację niż inne formy trójwartościowego chromu, ale wyniki te są również przedmiotem dyskusji. Obawy te opierały się częściowo na badaniach na muszkach owocowych, u których suplementacja pikolinianem chromu(III) powoduje aberracje chromosomalne, utrudnia rozwój potomstwa oraz powoduje bezpłodność i mutacje śmiertelne.
Opublikowano badanie oceniające toksyczność pikolinianu Cr(III) u ludzi. Naukowcy, którzy przeprowadzili to badanie, wykorzystali wcześniejszą wiedzę, że Cr(III) jest redukowany do Cr(II) przez komórkowe reduktory, takie jak NADH lub cysteina . Ta forma zredukowana Cr (II) przedstawiono na reakcji z H 2 O 2 do wytworzenia rodników , które z kolei utlenia par zasad DNA . Mając na uwadze tę wiedzę, naukowcy podawali dziesięciu kobietom 400 μg pikolinianu chromu(III) dziennie przez okres ośmiu tygodni. Mierząc ilość utlenionej pary zasad DNA, 5-hydroksymetylouracylu przy użyciu mian przeciwciał , grupa może wywnioskować ilość utlenienia pary zasad DNA zachodzącego w bezpośrednim związku z pikolinianem chromu(III). Wyniki badania sugerowały, że sam pikolinian chromu(III) nie powoduje istotnych uszkodzeń chromosomów in vivo .
Ogólnie rzecz biorąc, wykazano, że pikolinian chromu(III) nie jest toksyczny dla ludzi. W przypadku większości dorosłych można go przyjmować doustnie w dawkach do 1000 μg dziennie. Ta niska toksyczność jest ogólnie związana z niską absorbancją Cr(III) w organizmie przez płuca , skórę i przewód pokarmowy , połączoną z wysokim wydalaniem. Normalnie 99% pobranego chromu(III) można odzyskać z kałem użytkownika. Odnotowano pojedyncze przypadki suplementacji chromu(III) prowadzące do niewydolności nerek, jednak związek ten jest niejasny i nie został jeszcze zbadany.
Regulacja pikolinianu chromu(III)
W 2004 r. brytyjska Agencja ds. Standardów Żywności zaleciła konsumentom stosowanie innych form trójwartościowego chromu zamiast pikolinianu chromu(III) do czasu uzyskania specjalistycznej porady z Komitetu ds. Mutagenności. Było to spowodowane obawami podniesionymi przez Grupę Ekspertów ds. Witamin i Minerałów, że pikolinian chromu(III) może być genotoksyczny (powodować raka). Komitet odnotował również dwa doniesienia o przypadkach niewydolności nerek, które mogły być spowodowane przez ten suplement i wezwał do dalszych badań nad jego bezpieczeństwem. W grudniu 2004 r. Komitet ds. Mutagenności opublikował swoje ustalenia, w których stwierdził, że „ogólnie można stwierdzić, że bilans danych sugeruje, iż pikolinian chromu(III) nie powinien być uważany za mutagenny in vitro” oraz że „dostępne w -testy vivo u ssaków z pikolinianem chromu(III) są ujemne”. Po tych ustaleniach brytyjska Agencja ds. Standardów Żywności wycofała swoje zalecenia dotyczące unikania pikolinianu chromu(III), chociaż planuje kontynuować przegląd swoich zaleceń dotyczących suplementów chromu.
W 2010 r. pikolinian chromu(III) został zatwierdzony przez Health Canada do stosowania w suplementach diety. Zatwierdzone oświadczenia na etykietach obejmują: czynnik w utrzymaniu dobrego stanu zdrowia, zapewnia wsparcie dla zdrowego metabolizmu glukozy, pomaga organizmowi w metabolizowaniu węglowodanów i pomaga organizmowi w metabolizowaniu tłuszczów.
Bibliografia
Zewnętrzne linki
-
 Multimedia związane z pikolinianem chromu (III) w Wikimedia Commons
Multimedia związane z pikolinianem chromu (III) w Wikimedia Commons - Instrukcja Merck







