Kwas kakodylowy - Cacodylic acid

|
|
|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Kwas dimetyloarsynowy |
|
| Inne nazwy
Kwas dimetylarsenowy, kwas kakodylowy, tlenek hydroksydimetyloarsyny, Arsecodile, Ansar, Silvisar, Phytar 560, DMAA, UN 1572
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 1736965 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Karta informacyjna ECHA |
100.000,804 |
| Numer WE | |
| 130562 | |
| KEGG | |
|
PubChem CID
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 1572 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 2 H 7 AsO 2 | |
| Masa cząsteczkowa | 137,9977 g / mol |
| Wygląd | Białe kryształy lub proszek |
| Zapach | bezwonny |
| Gęstość | > 1,1 g / cm 3 |
| Temperatura topnienia | 192 do 198 ° C (378 do 388 ° F; 465 do 471 K) |
| Temperatura wrzenia | > 200 ° C (392 ° F, 473 K) |
| 66,7 g / 100 ml | |
| Rozpuszczalność | rozpuszczalny w etanolu , kwas octowy nierozpuszczalny w eterze dietylowym |
| Kwasowość (p K a ) | 6 |
| -79,9 · 10-6 cm 3 / mol | |
| Struktura | |
| trójskośny | |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna karta charakterystyki |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Niebezpieczeństwo |
| H301 , H331 , H400 , H410 | |
| P261 , P264 , P270 , P271 , P273 , P301 + 310 , P304 + 340 , P311 , P321 , P330 , P391 , P403 + 233 , P405 , P501 | |
| NFPA 704 (ognisty diament) | |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
700 mg / kg (szczur, doustnie) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
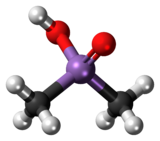
Kwas kakodylowy jest związkiem organoarsenowym o wzorze (CH 3 ) 2 AsO 2 H. O wzorze R 2 As (O) OH jest najprostszym z kwasów arsynoorganicznych . Jest to bezbarwne ciało stałe rozpuszczalne w wodzie.
W wyniku neutralizacji kwasu kakodylowego zasadą otrzymuje się sole kakodylanów , np . Kakodylan sodu . Są silnymi herbicydami . Kwas kakodylowy / kakodylan sodu jest środkiem buforującym w przygotowaniu i utrwalaniu próbek biologicznych do mikroskopii elektronowej .
Historia
W XVIII wieku stwierdzono, że połączenie As 2 O 3 i czterech równoważników octanu potasu (CH 3 CO 2 K) daje produkt zwany „ dymiącym płynem kadeta ”, który zawiera tlenek kakodylu ((CH 3 ) 2 As) 2 O i kakodyl , ((CH 3 ) 2 As) 2 .
Wczesne badania nad " kakodylami " zostały opisane przez Roberta Bunsena na Uniwersytecie w Marburgu. Bunsen powiedział o związkach: „zapach tego ciała wywołuje natychmiastowe mrowienie w dłoniach i stopach, a nawet zawroty głowy i nieczułość… Jest godne uwagi, że kiedy ktoś jest wystawiony na zapach tych związków, język pokrywa się czernią powłoka, nawet jeśli dalsze złe efekty nie są zauważalne ”. Jego praca w tej dziedzinie doprowadziła do lepszego zrozumienia grupy metylowej .
Tlenek kakodylu ((CH 3 ) 2 As) 2 O jest często uważany za pierwszy związek metaloorganiczny wytwarzany syntetycznie.
Kwas kakodylowy i jego sole były dodawane do herbicydów przez wielu różnych producentów pod różnymi nazwami handlowymi. Firma APC Holdings Corp. sprzedawała kwas kakodylowy i jego sole pod marką Phytar. Odmianą używaną w Wietnamie (jako Agent Blue ) był Phytar 560G. „ Agent Blue ”, mieszanina kwasu kakodylowego i kakodylanu sodu, była używana podczas wojny w Wietnamie jako defoliantu.
Reakcje
Kwas Kakodylowy jest słaby kwas o pK a 6.
Kwas kakodylowy można zredukować do dimetyloarsyny, która jest wszechstronnym półproduktem do syntezy innych związków organoarsenowych:
- (CH 3 ) 2 AsO 2 H + 2 Zn + 4 HCl → (CH 3 ) 2 AsH + 2 ZnCl 2 + 2 H 2 O
- (CH 3 ) 2 AsO 2 H + SO 2 + HI → (CH 3 ) 2 AsI + SO 3 + H 2 O
Efekty zdrowotne
Kwas kakodylowy jest silnie toksyczny w przypadku spożycia, wdychania lub kontaktu ze skórą. Amerykańska Agencja Ochrony Środowiska stwierdza, że wszystkie formy arsenu są poważnym zagrożeniem dla zdrowia ludzkiego, a Agencja ds. Substancji Toksycznych i Rejestru Chorób Stanów Zjednoczonych umieściła arszenik na pierwszym miejscu w swojej Priorytetowej Liście Substancji Niebezpiecznych z 2001 r. W lokalizacjach Superfund. Arsen jest klasyfikowany jako Group-A rakotwórczy .
Zobacz też
Bibliografia
- ^ Stanley A. Greene (2005). Sittig's Handbook of Pesticides and Agricultural Chemicals . Williama Andrew. p. 132. ISBN 978-0-8155-1903-4 .
- ^ Komitet do przeglądu skutków zdrowotnych weteranów narażenia na herbicydy w Wietnamie; Instytut Medycyny (1994). Veterans and Agent Orange: Health Effects of Herbicides Used in Vietnam . National Academies Press. s. 89–90. ISBN 978-0-309-55619-4 .
- ^ Henry BFDixon (1996). „Biochemiczne działanie kwasów podpalających, zwłaszcza analogów fosforanów”. Postępy w chemii nieorganicznej . Postępy w chemii nieorganicznej. 44 . s. 191–227. doi : 10.1016 / S0898-8838 (08) 60131-2 . ISBN 9780120236442 .
- ^ Feltham, RD; Kasenally, A .; Nyholm, RS (1967). „Nowa synteza dwu- i trójrzędowych arsynów”. Journal of Organometallic Chemistry . 7 (2): 285–288. doi : 10.1016 / S0022-328X (00) 91079-9 . CS1 maint: używa parametru autorów ( link )
- ^ Burrows, GJ i Turner, EE, „Nowy typ związku zawierającego arszenik”, Journal of the Chemical Society Transactions, 1920, 1374-1383
- ^ a b Dibyendu, Sarkar; Datta, Rupali (2007). „Biogeochemia arsenu w skażonych glebach terenów Superfund” . EPA . Agencja Ochrony Środowiska Stanów Zjednoczonych . Źródło 25 lutego 2018 r .
- Kenyon, EM; Hughes, MF (2001). „A Concise Review of the Toxicity and Carcinogenicity of Dimethylarsenic Acid” . Toksykologia . 160 (1–3): 227–236. doi : 10.1016 / S0300-483X (00) 00458-3 . PMID 11246143 .
- Elschenbroich, C; Salzer, A. (1992) Organometallics, 2nd Edition
- Biografia Bunsena

