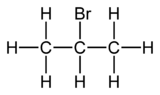
2-bromopropan - 2-Bromopropane

|
|||
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
2-bromopropan |
|||
| Inne nazwy
Bromek izopropylu
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| 741852 | |||
| ChEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.000.778 |
||
| Numer WE | |||
| Siatka | 2-bromopropan | ||
|
PubChem CID
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 2344 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 3 H 7 Br | |||
| Masa cząsteczkowa | 122,993 g · mol -1 | ||
| Wygląd | Bezbarwna ciecz | ||
| Gęstość | 1,31 g ml -1 | ||
| Temperatura topnienia | -89,0 ° C; -128,1 ° F; 184,2 K | ||
| Temperatura wrzenia | Od 59 do 61 ° C; Od 138 do 142 ° F; 332 do 334 K | ||
| 3,2 g L −1 (przy 20 ° C) | |||
| log P | 2.136 | ||
| Ciśnienie pary | 32 kPa (przy 20 ° C) | ||
|
Stała prawa Henry'ego ( k H ) |
1,0 μmol Pa −1 mol −1 | ||
|
Współczynnik załamania ( n D )
|
1.4251 | ||
| Lepkość | 0,4894 mPa s (przy 20 ° C) | ||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
135,6 JK mol −1 | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
−129 kJ mol −1 | ||
|
Standardowa entalpia
spalania (Δ c H ⦵ 298 ) |
−2,0537–−2,0501 MJ mol −1 | ||
| Zagrożenia | |||
| Piktogramy GHS |
 
|
||
| Hasło ostrzegawcze GHS | Niebezpieczeństwo | ||
| H225 , H360 , H373 | |||
| P210 , P308 + 313 | |||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | 19 ° C (66 ° F, 292 K) | ||
| Związki pokrewne | |||
|
Powiązane alkany
|
|||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencje Infobox | |||
2-Bromopropan , znany również jako bromek izopropylu i bromku 2-propylu , jest halogenowany węglowodór o wzorze CH 3 CHBrCH 3 . Jest to bezbarwna ciecz. Służy do wprowadzania izopropylowej grupy funkcyjnej w syntezie organicznej . 2-bromopropan wytwarza się przez ogrzewanie izopropanolu z kwasem bromowodorowym .
Przygotowanie
2-Bromopropan jest dostępny w handlu. Można go otrzymać w zwykły sposób z bromków alkilu, w reakcji izopropanolu z fosforem i bromem lub z trójbromkiem fosforu .
Bezpieczeństwo
Krótkołańcuchowe halogenki alkilu są często rakotwórcze .
Bromu atomem znajduje się w położeniu, które umożliwia wtórne cząsteczka poddać dehydrohalogenowanie łatwo dają propen , który ulatnia się w postaci gazu i można rozerwać zamkniętych naczyniach reakcyjnych. Gdy ten odczynnik jest używany w reakcjach katalizowanych zasadą, zamiast wodorotlenku sodu lub potasu należy użyć węglanu potasu .
Dalsza lektura
- M G. Gergel „Przepraszam, czy chciałbyś kupić kilogram bromku izopropylu?” Pierce Chemical Co. (1979). (historia start-upu firmy chemicznej).



