Fluoren - Fluorene
|
|

|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
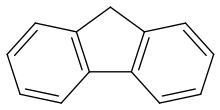
9 H -fluoren |
|
|
Systematyczna nazwa IUPAC
Tricyklo[7.4.0.0 2,7 ]trideka-2,4,6,9,11,13-heksaen |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA |
100.001.541 |
| Numer WE | |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 13 H 10 | |
| Masa cząsteczkowa | 166,223 g·mol -1 |
| Gęstość | 1,202 g/ml |
| Temperatura topnienia | 116 do 117 °C (241 do 243 °F; 389 do 390 K) |
| Temperatura wrzenia | 295 ° C (563 ° F; 568 K) |
| 1,992 mg/l | |
| Rozpuszczalność | rozpuszczalniki organiczne |
| log P | 4.18 |
| Kwasowość (p K a ) | 22,6 |
| -110,5 x 10 -6 cm 3 / mol | |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | Sigma-Aldrich |
| NFPA 704 (ognisty diament) | |
| Temperatura zapłonu | 152 ° C (306 ° F; 425 K) |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
16000 mg/kg (doustnie, szczur) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Fluoren / F l ʊər ı n / , albo 9 H -fluoreno jest organiczny związek o wzorze (C 6 H 4 ) 2 CH 2 . Tworzy białe kryształy o charakterystycznym aromatycznym zapachu podobnym do zapachu naftalenu . Posiada fioletową fluorescencję , stąd jej nazwa. W celach handlowych pozyskiwany jest ze smoły węglowej . Jest nierozpuszczalny w wodzie i rozpuszczalny w wielu rozpuszczalnikach organicznych. Chociaż czasami jest klasyfikowany jako wielopierścieniowy węglowodór aromatyczny , pięcioczłonowy pierścień nie ma właściwości aromatycznych. Fluoren jest lekko kwaśny.
Synteza, struktura i reaktywność
Chociaż fluoren otrzymuje się ze smoły węglowej, można go również otrzymać przez odwodornienie difenylometanu . Alternatywnie, można go otrzymać przez redukcję fluorenon z cynkiem . Cząsteczka fluorenu jest prawie płaska, chociaż każdy z dwóch pierścieni benzenowych jest współpłaszczyznowy z centralnym węglem 9.
Kwasowość
Miejsca C9-H o fluoren pierścienia są słabo kwaśnym ( wartość pKa = 22,6 w DMSO ). Deprotonowanie daje stabilny fluorenylowej anion, nominalnie C 13 H 9 - , która jest aromatyczny i posiada intensywny kolor pomarańczowy. Anion jest nukleofilem . Elektrofile reagują z nim dodając do pozycji 9. Oczyszczanie fluorenu wykorzystuje jego kwasowość i niską rozpuszczalność jego pochodnej sodowej w rozpuszczalnikach węglowodorowych.
Oba protony można usunąć z C9. Na przykład 9,9-fluorenylodipotas można otrzymać działając na fluoren metalicznym potasem we wrzącym dioksanie .
Właściwości liganda
Fluoren i jego pochodne mogą być deprotonowane z wytworzeniem ligandów podobnych do cyklopentadienidu .

Zastosowania
Fluoren jest prekursorem innych związków fluorenu; gatunek rodzicielski ma niewiele zastosowań. Kwas fluoreno-9-karboksylowy jest prekursorem farmaceutyków. Utlenianie fluorenu daje fluorenon , który poddaje się nitrowaniu w celu uzyskania handlowo użytecznych pochodnych. Chloromrówczan 9-fluorenylometylu (chlorek Fmoc) stosuje się do wprowadzenia grupy zabezpieczającej karbaminianu 9-fluorenylometylu (Fmoc) do amin w syntezie peptydów .
Polimery polifluorenu (gdzie węgiel 7 jednej jednostki jest połączony z węglem 2 drugiej jednostki, wypierając dwa wodory) są elektrycznie przewodzące i elektroluminescencyjne i były szeroko badane jako luminofor w organicznych diodach elektroluminescencyjnych .
Barwniki fluorenowe
Barwniki fluorenowe są dobrze rozwinięte. Większość wytwarza się przez kondensację aktywnej grupy metylenowej z karbonylkami. Prekursorami barwników są 2-aminofluoren, 3,6-bis-(dimetyloamino)fluoren i 2,7-dijodofluoren.
Zobacz też
Bibliografia
Linki zewnętrzne
- Fluoren w bazie danych National Institute of Standards and Technology.

