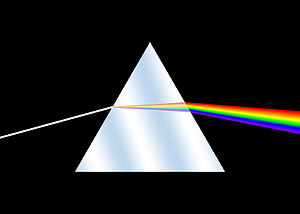
Historia spektroskopii - History of spectroscopy
Współczesna spektroskopia w świecie zachodnim rozpoczęła się w XVII wieku. Nowe konstrukcje w optyce , w szczególności pryzmaty , umożliwiły systematyczne obserwacje widma słonecznego . Isaac Newton pierwszy zastosował słowo spektrum opisać tęczę z kolorów , które łączą się tworząc białe światło. Na początku XIX wieku Joseph von Fraunhofer prowadził eksperymenty ze spektrometrami dyspersyjnymi , dzięki którym spektroskopia stała się bardziej precyzyjną i ilościową techniką naukową. Od tego czasu spektroskopia odgrywała i nadal odgrywa znaczącą rolę w chemii , fizyce i astronomii . Fraunhofer zaobserwował i zmierzył ciemne linie w widmie Słońca , które teraz noszą jego imię, chociaż kilka z nich zaobserwował wcześniej Wollaston .
Geneza i rozwój eksperymentalny
Rzymianie znali już zdolność pryzmatu do generowania tęczy kolorów. Newton jest tradycyjnie uważany za twórcę spektroskopii, ale nie był pierwszym naukowcem, który badał i opisywał widmo słoneczne. Prace Athanasius Kircher (1646), Jana Marka Marci (1648), Roberta Boyle (1664) i Francesco Marii Grimaldi (1665) poprzedzają eksperymenty optyczne Newtona (1666–1672). Newton opublikował swoje eksperymenty i teoretyczne wyjaśnienia dyspersji światła w swoich Optykach . Jego eksperymenty wykazały, że białe światło można rozbić na składowe kolory za pomocą pryzmatu i że te składniki można ponownie połączyć, aby wygenerować białe światło. Pokazał, że pryzmat nie nadaje ani nie tworzy kolorów, ale raczej oddziela części składowe światła białego. Korpuskularna teoria światła Newtona została stopniowo zastąpiona teorią falową . Dopiero w XIX wieku rozpoznano i ustandaryzowano ilościowy pomiar światła rozproszonego. Podobnie jak w przypadku wielu późniejszych eksperymentów spektroskopowych, źródła białego światła Newtona obejmowały płomienie i gwiazdy , w tym Słońce . Kolejne badania natury światła obejmują prace Hooke'a , Huygensa , Younga . Kolejne eksperymenty z pryzmatami dostarczyły pierwszych wskazówek, że widma są jednoznacznie związane ze składnikami chemicznymi. Naukowcy zaobserwowali emisję wyraźnych wzorów kolorów, gdy do płomieni alkoholowych dodano sole .
Początek XIX wieku (1800-1829)
W 1802 roku William Hyde Wollaston zbudował spektrometr, udoskonalając model Newtona, który zawierał soczewkę skupiającą widmo Słońca na ekranie. Po użyciu Wollaston zdał sobie sprawę, że kolory nie były rozłożone równomiernie, ale zamiast tego miały brakujące plamy kolorów, które wyglądały jak ciemne pasma w widmie słonecznym. W tym czasie Wollaston wierzył, że te linie są naturalnymi granicami między kolorami, ale hipoteza ta została później wykluczona w 1815 roku przez pracę Fraunhofera.
Joseph von Fraunhofer dokonał znaczącego skoku eksperymentalnego, zastępując pryzmat siatką dyfrakcyjną jako źródłem dyspersji długości fal . Fraunhofer zbudował teorie interferencji światła opracowane przez Thomasa Younga , François Arago i Augustina-Jeana Fresnela . Przeprowadził własne eksperymenty, aby zademonstrować efekt przepuszczania światła przez pojedynczą prostokątną szczelinę, dwie szczeliny i tak dalej, ostatecznie opracowując metodę gęstego rozmieszczenia tysięcy szczelin w celu utworzenia siatki dyfrakcyjnej. Interferencja uzyskana przez siatkę dyfrakcyjną zarówno poprawia rozdzielczość widmową na pryzmacie, jak i pozwala na ilościowe określenie rozproszonych długości fal. Ustalenie przez Fraunhofera ilościowej skali długości fal utorowało drogę do dopasowania widm obserwowanych w wielu laboratoriach, z wielu źródeł (płomienie i słońce) oraz za pomocą różnych instrumentów. Fraunhofer dokonał i opublikował systematyczne obserwacje widma słonecznego, a ciemne pasma, które zaobserwował i określił długości fal, są nadal znane jako linie Fraunhofera .
Na początku XIX wieku wielu naukowców posuwało naprzód techniki i zrozumienie spektroskopii. W latach dwudziestych XIX wieku zarówno John Herschel , jak i William HF Talbot prowadzili systematyczne obserwacje soli za pomocą spektroskopii płomieniowej .
Połowa XIX wieku (1830-1869)
W 1835 roku Charles Wheatstone poinformował, że różne metale można łatwo odróżnić dzięki różnym jasnym liniom w widmach emisyjnych ich iskier , wprowadzając w ten sposób alternatywny mechanizm do spektroskopii płomieniowej. W 1849 r. JBL Foucault wykazał eksperymentalnie, że linie absorpcji i emisji pojawiające się przy tej samej długości fali są spowodowane tym samym materiałem, a różnica między nimi wynika z temperatury źródła światła. W 1853 roku szwedzki fizyk Anders Jonas Ångström przedstawił obserwacje i teorie dotyczące widm gazu w swojej pracy Optiska Undersökningar (Badania optyczne) Królewskiej Szwedzkiej Akademii Nauk . Ångström postulował, że rozżarzony gaz emituje promienie świetlne o tej samej długości fali, co te, które może pochłonąć. Ångström nie znał wyników eksperymentalnych Foucalta. W tym samym czasie o podobnych postulatach dyskutowali George Stokes i William Thomson (Kelvin) . Ångström zmierzył również widmo emisyjne wodoru, które później nazwano liniami Balmera . W 1854 i 1855 David Alter opublikował obserwacje widm metali i gazów, w tym niezależną obserwację linii Balmera dla wodoru.
Systematyczne przypisywanie widm pierwiastkom chemicznym rozpoczęło się w latach 60. XIX wieku dzięki pracy niemieckich fizyków Roberta Bunsena i Gustava Kirchhoffa , którzy odkryli, że linie Fraunhofera odpowiadają liniom widma emisji obserwowanym w laboratoryjnych źródłach światła. To utorowało drogę do analizy spektrochemicznej w naukach laboratoryjnych i astrofizycznych. Bunsen i Kirchhoff zastosowali techniki optyczne Fraunhofera, ulepszone źródło płomienia Bunsena, oraz wysoce systematyczną procedurę eksperymentalną do szczegółowego badania widm związków chemicznych. Ustanowili powiązanie między pierwiastkami chemicznymi a ich unikalnymi wzorcami widmowymi. W tym procesie opracowali technikę spektroskopii analitycznej. W 1860 roku opublikowali swoje odkrycia dotyczące widm ośmiu pierwiastków i zidentyfikowali obecność tych pierwiastków w kilku naturalnych związkach. Wykazali, że spektroskopię można wykorzystać do śladowej analizy chemicznej, a kilka odkrytych przez nich pierwiastków chemicznych było wcześniej nieznanych. Kirchhoff i Bunsen również definitywnie ustalili powiązanie między liniami absorpcji i emisji, w tym przypisanie linii absorpcji słonecznej poszczególnym pierwiastkom na podstawie ich widm. Kirchhoff kontynuował prace nad podstawowymi badaniami natury absorpcji i emisji spektralnej, w tym tak zwanym prawem promieniowania cieplnego Kirchhoffa . Zastosowania Kirchhoffa tego prawa do spektroskopii ujęte są w trzech prawach spektroskopii :
- Rozżarzone ciało stałe, ciecz lub gaz pod wysokim ciśnieniem emituje ciągłe widmo .
- Gorący gaz pod niskim ciśnieniem emituje widmo „jasnej linii” lub linii emisyjnej.
- Ciągłe źródło widma oglądane przez chłodny gaz o małej gęstości wytwarza widmo w linii absorpcyjnej.
W latach 60. XIX wieku małżeństwo Williama i Margaret Huggins wykorzystało spektroskopię do ustalenia, że gwiazdy składają się z tych samych elementów, które znajdują się na Ziemi. Wykorzystali również nierelatywistyczne równanie przesunięcia Dopplera ( przesunięcie ku czerwieni ) na widmie gwiazdy Syriusza w 1868 roku, aby określić jej prędkość osiową. Jako pierwsi pobrali widmo mgławicy planetarnej podczas analizy Mgławicy Kocie Oko (NGC 6543). Korzystając z technik spektralnych, byli w stanie odróżnić mgławice od gwiazd.
August Beer zaobserwował związek pomiędzy absorpcją światła a koncentracją i stworzył komparator kolorów, który później został zastąpiony dokładniejszym urządzeniem zwanym spektrofotometrem .
Koniec XIX wieku (1870-1899)
W XIX wieku nowe osiągnięcia, takie jak odkrycie fotografii, wynalezienie przez Rowlanda wklęsłej siatki dyfrakcyjnej oraz prace Schumanna nad odkryciem próżniowego ultrafioletu (fluoryt do pryzmatów i soczewek, klisze fotograficzne o niskiej zawartości żelatyny i absorpcja UV w powietrzu poniżej 185 nm ) bardzo szybko przeszły na krótsze fale. W tym samym czasie Dewar obserwował serie w widmach alkalicznych, Hartley znalazł stałe różnice w liczbach fal , Balmer odkrył zależność łączącą długości fal w widmie wodoru widzialnego, a wreszcie Rydberg wyprowadził wzór na liczby falowe serii widmowych.
Johann Balmer odkrył w 1885 roku, że cztery widoczne linie wodoru są częścią serii, którą można wyrazić w liczbach całkowitych. Kilka lat później pojawiła się formuła Rydberga , opisująca dodatkowe serie linii.
Tymczasem obszerne podsumowanie dotychczasowych eksperymentów wykonanych przez Maxwella (1873) zaowocowało jego równaniami fal elektromagnetycznych .
W 1895 roku niemiecki fizyk Wilhelm Conrad Röntgen odkrył i intensywnie badał promieniowanie rentgenowskie , które później wykorzystano w spektroskopii rentgenowskiej . Rok później, w 1896 roku, francuski fizyk Antoine Henri Becquerel odkrył radioaktywność, a holenderski fizyk Pieter Zeeman zaobserwował rozszczepianie linii widmowych przez pole magnetyczne.
W 1897 roku fizyk teoretyczny Joseph Larmor wyjaśnił rozszczepienie linii widmowych w polu magnetycznym przez drgania elektronów.
Fizyk Joseph Larmor stworzył pierwszy model atomu w Układzie Słonecznym w 1897 roku. Postulował także proton, nazywając go „elektronem dodatnim”. Powiedział, że zniszczenie tego typu atomu tworzącego materię „jest zjawiskiem o nieskończenie małym prawdopodobieństwie”.
Początek XX wieku (1900-1950)
Pierwsza dekada XX wieku przyniosła podstawy teorii kwantowej ( Planck , Einstein ) oraz interpretację szeregu widmowego wodoru przez Lymana w VUV i Paschena w podczerwieni . Ritz sformułował zasadę łączenia .
W 1913 Bohr sformułował swój kwantowo-mechaniczny model atomu. Stymulowało to empiryczną analizę terminów. Bohr opublikował teorię atomów wodoropodobnych, która może wyjaśnić obserwowane długości fal linii widmowych z powodu przejścia elektronów z różnych stanów energetycznych. W 1937 roku „E. Lehrer stworzył pierwszy w pełni zautomatyzowany spektrometr”, aby pomóc dokładniej mierzyć linie spektralne. Dzięki opracowaniu bardziej zaawansowanych instrumentów, takich jak fotodetektory, naukowcy byli w stanie dokładniej mierzyć absorpcję substancji o określonej długości fali.
Rozwój mechaniki kwantowej
W latach 1920-1930 podstawowe koncepcje mechaniki kwantowej opracowali Pauli , Heisenberg , Schrödinger i Dirac . Zrozumienie zasady spinu i wykluczenia pozwoliło na wyobrażenie sobie, w jaki sposób powłoki elektronowe atomów wypełniane są rosnącą liczbą atomową .
Pomnóż zjonizowane atomy
Ta gałąź spektroskopii zajmuje się promieniowaniem związanym z atomami pozbawionymi kilku elektronów (wielokrotnie zjonizowane atomy (MIA), wielokrotnie naładowane jony, wysoko naładowane jony ). Są one obserwowane w bardzo gorącej plazmie (laboratoryjnej lub astrofizycznej) lub w eksperymentach akceleratorowych ( wiązka-folia , pułapka jonowa z wiązką elektronów (EBIT)). Najniżej wychodzące powłoki elektronowe takich jonów rozpadają się do stabilnych stanów podstawowych wytwarzając fotony w obszarach widmowych VUV , EUV i miękkiego promieniowania rentgenowskiego (tzw. przejścia rezonansowe).
Studia strukturalne
Dalszy postęp w badaniach struktury atomowej był ściśle powiązany z postępem w kierunku krótszych długości fal w regionie EUV. Millikan , Sawyer , Bowen użyli wyładowań elektrycznych w próżni, aby zaobserwować pewne linie widmowe emisji do 13 nm, które zalecali atomom pozbawionym warstwy. 1927 Osgooda i Hoag podano w grazing incidence wklęsłe tarcia spektrografy i fotografowano linii do 4,4 nm, (K alfa węgla). Dauvillier użył kryształu kwasu tłuszczowego o dużej przestrzeni siatki krystalicznej, aby rozszerzyć widma miękkiego promieniowania rentgenowskiego do 12,1 nm, a luka została zamknięta. W tym samym okresie Manne Siegbahn skonstruował bardzo wyrafinowany spektrograf padania padającego, który umożliwił Ericsonowi i Edlénowi uzyskanie wysokiej jakości widm iskry próżniowej i niezawodnej identyfikacji linii zwielokrotnionych zjonizowanych atomów aż do O VI, z pięcioma pozbawionymi elektronów. Grotrian opracował graficzną prezentację struktury energetycznej atomów. Russel i Saunders zaproponowali swój schemat sprzężenia dla interakcji spin-orbita i ich ogólnie uznaną notację dla terminów spektralnych .
Precyzja
Teoretyczne obliczenia kwantowo-mechaniczne stają się dość dokładne, aby opisać strukturę energetyczną niektórych prostych konfiguracji elektronicznych. Wyniki prac teoretycznych zostały podsumowane przez Condona i Shortleya w 1935 roku.
Edlén dokładnie przeanalizował widma MIA dla wielu pierwiastków chemicznych i wyprowadził regularności w strukturach energetycznych MIA dla wielu sekwencji izoelektronowych (jony o tej samej liczbie elektronów, ale różnych ładunkach jądrowych). Zaobserwowano widma dość wysokich stopni jonizacji (np. Cu XIX).
Najbardziej ekscytujące wydarzenie miało miejsce w 1942 roku, kiedy Edlén udowodnił identyfikację niektórych słonecznych linii koronalnych na podstawie swoich precyzyjnych analiz widm MIA. Sugerowało to, że korona słoneczna ma temperaturę miliona stopni i silnie zaawansowane rozumienie fizyki Słońca i gwiazd.
Po II wojnie światowej rozpoczęto eksperymenty na balonach i rakietach, aby obserwować promieniowanie VUV Słońca. (Patrz astronomia rentgenowska ). Od 1960 r. kontynuowano intensywniejsze badania, w tym spektrometry na satelitach.
W tym samym okresie spektroskopia laboratoryjna MIA staje się istotna jako narzędzie diagnostyczne dla gorącej plazmy urządzeń termojądrowych (patrz Fuzja jądrowa ), która rozpoczęła się wraz z budową Stellaratora w 1951 roku przez Spitzera, a kontynuowana była z tokamakami , skurczami- z i plazmą wytwarzaną laserem. Postęp w akceleratorach jonowych stymulował spektroskopię wiązek-folii jako środek do pomiaru czasu życia stanów wyjściowych MIA. Uzyskano wiele różnych danych dotyczących poziomów energetycznych o wysokim poziomie wyjściowym , stanów autojonizacji i jonizacji wewnętrznego rdzenia.
Pułapka jonowa wiązki elektronów
Jednocześnie podejścia teoretyczne i obliczeniowe dostarczyły danych niezbędnych do identyfikacji nowych widm i interpretacji obserwowanych natężeń linii. Nowe dane laboratoryjne i teoretyczne stają się bardzo przydatne do obserwacji spektralnych w kosmosie. To był prawdziwy przełom w pracach nad MIA w USA, Anglii, Francji, Włoszech, Izraelu, Szwecji, Rosji i innych krajach
Nową stronę w spektroskopii MIA można datować na rok 1986 wraz z rozwojem EBIT (Levine i Marrs, LLNL ) dzięki korzystnej kompozycji nowoczesnych zaawansowanych technologii, takich jak kriogenika , ultrawysoka próżnia , magnesy nadprzewodzące , potężne wiązki elektronów i półprzewodniki detektory . Bardzo szybko stworzono źródła EBIT w wielu krajach (patrz podsumowanie NIST, aby uzyskać wiele szczegółów, a także recenzje).
Możliwy jest szeroki zakres badań spektroskopowych z EBIT, w tym osiąganie najwyższych stopni jonizacji (U 92+ ), pomiar długości fali, nadsubtelna struktura poziomów energetycznych, kwantowe badania elektrodynamiczne , pomiary przekrojów jonizacyjnych (CS), wzbudzanie udarem elektronowym CS , polaryzacja promieniowania rentgenowskiego , względne natężenia linii, rekombinacja dielektroniczna CS, rozpad oktupola magnetycznego, czasy życia zabronionych przejść , rekombinacja wymiany ładunku itp.
Spektroskopia w podczerwieni i Ramana
Wielu wczesnych naukowców, którzy badali widma związków w podczerwieni, musiało opracować i zbudować własne instrumenty, aby móc rejestrować swoje pomiary, co bardzo utrudniało uzyskanie dokładnych pomiarów. Podczas II wojny światowej rząd Stanów Zjednoczonych zlecił różnym firmom opracowanie metody polimeryzacji butadienu w celu wytworzenia kauczuku , ale można było to zrobić tylko poprzez analizę izomerów węglowodorów Ca. Te zakontraktowane firmy zaczęły opracowywać instrumenty optyczne i ostatecznie stworzyły pierwsze spektrometry na podczerwień. Wraz z rozwojem tych komercyjnych spektrometrów Spektroskopia w podczerwieni stała się bardziej popularną metodą określania „odcisku palca” dla dowolnej cząsteczki. Spektroskopię Ramana po raz pierwszy zaobserwował w 1928 r. Sir Chandrasekhara Venkata Raman w substancjach ciekłych, a także „Grigory Landsberg i Leonid Mandelstam w kryształach”. Spektroskopia Ramana opiera się na obserwacji efektu Ramana, który jest definiowany jako „Intensywność rozproszonego światła zależy od wielkości zmiany potencjału polaryzacji”. Widmo Ramana rejestruje natężenie światła w funkcji częstotliwości światła (liczba falowa), a przesunięcie liczby falowej jest charakterystyczne dla każdego indywidualnego związku.
Spektroskopia laserowa
Spektroskopia laserowa to technika spektroskopowa, która wykorzystuje lasery do określenia częstotliwości emitowanej materii. Laser został wynaleziony, ponieważ spektroskopiści przyjęli koncepcję jego poprzednika, masera , i zastosowali go do zakresów światła widzialnego i podczerwonego. Maser został wynaleziony przez Charlesa Townesa i innych spektroskopów, aby stymulować materię w celu określenia częstotliwości promieniowania emitowanych przez określone atomy i cząsteczki. Podczas pracy nad maserem Townes zdał sobie sprawę, że możliwe są dokładniejsze detekcje wraz ze wzrostem częstotliwości emitowanej mikrofali. Kilka lat później narodził się pomysł wykorzystania widzialnego i ostatecznie podczerwonego zakresu światła do spektroskopii, który z pomocą Arthura Schawlowa stał się rzeczywistością . Od tego czasu lasery znacznie przyczyniły się do postępu w spektroskopii eksperymentalnej. Światło laserowe pozwoliło na znacznie większą precyzję eksperymentów, szczególnie w zastosowaniach badania kolizji światła, a także na dokładne wykrywanie określonych długości fal i częstotliwości światła, co pozwoliło na wynalezienie urządzeń, takich jak laserowe zegary atomowe. Lasery stworzyły również spektroskopię, która wykorzystywała metody czasowe dokładniejsze, wykorzystując prędkości lub czasy zaniku fotonów przy określonych długościach fal i częstotliwościach, aby zachować czas. Techniki spektroskopii laserowej są wykorzystywane do wielu różnych zastosowań. Jednym z przykładów jest zastosowanie spektroskopii laserowej do wykrywania związków w materiałach. Jedna specyficzna metoda nazywa się spektroskopią fluorescencyjną indukowaną laserem i wykorzystuje metody spektroskopowe, aby móc wykryć, jakie materiały znajdują się w ciele stałym, ciekłym lub gazowym in situ . Pozwala to na bezpośrednie testowanie materiałów, zamiast zabierać materiał do laboratorium, aby dowiedzieć się, z czego składa się ciało stałe, ciecz lub gaz.