Kwas nadjodowy - Periodic acid
|
Kwas ortoperjodowy
|
|||
|
Kwas metaperiodowy
|
|||
 HIO 4 . 2 H 2 O
|
|||
| Nazwy | |||
|---|---|---|---|
| Inne nazwy | |||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.030.839 |
||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| HIO 4 (metaperiodyczny) H 5 IO 6 (ortoperiodyczny) |
|||
| Masa cząsteczkowa | 227,941 g/mol (H 5 IO 6 ) 190,91 g/mol (HIO 4 ) |
||
| Wygląd zewnętrzny | Bezbarwne kryształy | ||
| Temperatura topnienia | 128,5 ° C (263,3 ° F; 401,6 K) | ||
| Rozpuszczalność | rozpuszczalny w wodzie, alkoholach | ||
| Podstawa sprzężona | Nadjod | ||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna Karta Charakterystyki | ||
|
Klasyfikacja UE (DSD) (nieaktualna)
|
Utleniacz ( O ), Toksyczny ( T ), Żrący ( C ) | ||
| Zwroty R (nieaktualne) | R23 R24 R25 R34 R41 | ||
| NFPA 704 (ognisty diament) | |||
| Związki pokrewne | |||
|
Inne aniony
|
|||
|
Inne kationy
|
|||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
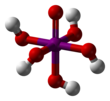
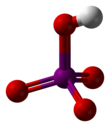
Kwas nadjodowy ( / ˌ P ɜːr aɪ ɒ d ɪ K / per Eye- OD -ik ) jest najwyżej kwasy tlenowe z jodem , w których występuje atom jodu w stanie utlenienia +7. Jak wszystkie nadjodany może występować w dwóch postaciach: kwasu ortoperiodowego o wzorze chemicznym H 5 I O 6 oraz kwasu metanadjodowego o wzorze HIO 4 .
Kwas nadjodowy został odkryty przez Heinricha Gustava Magnusa i CF Ammermüllera w 1833 roku.
Synteza
Nowoczesna produkcja na skalę przemysłową obejmuje utlenianie roztworu jodanu sodu w warunkach alkalicznych, albo elektrochemicznie na anodzie PbO 2 , albo przez traktowanie chlorem :
-
IO−
3+ 6 HO−
− 2 e − → IO5-
6+ 3 H 2 O ( dla przejrzystości pominięto przeciwjony ) E ° = -1,6 V -
IO−
3+ 6 HO−
+ CI 2 → IO5-
6+ 2 Cl − + 3 H 2 O
Kwas ortopeodowy można odwodnić z wytworzeniem kwasu metanadjodowego przez ogrzewanie do 100°C pod zmniejszonym ciśnieniem.
- H 5 IO 6 ⇌ HIO 4 + 2 H 2 O
Dalsze ogrzewanie do około 150°C daje raczej pięciotlenek jodu (I 2 O 5 ) niż oczekiwany bezwodnik heptoksyd dijodu (I 2 O 7 ). Kwas metanadjodowy można również wytworzyć z różnych ortonadjodanów przez traktowanie rozcieńczonym kwasem azotowym .
- H 5 IO 6 → HIO 4 + 2 H 2 O
Nieruchomości
Kwas ortopejodowy ma szereg stałych dysocjacji kwasu . Nie określono pKa kwasu metaperiodowego.
- H 5 IO 6 ⇌ H
4IO−
6+ H + , P K = 3,29
-
h
4IO−
6⇌ H
3IO2-
6+ H + , P K = 8,31
-
h
3IO2-
6⇌ H
2IO3-
6+ H + , P K = 11,60
Istnieją dwie formy kwasu nadjodowego, wynika z tego, że powstają dwa rodzaje soli nadjodowych. Na przykład, metanadjodan sodu , NalO 4 , mogą być syntetyzowane z HIO 4 podczas orthoperiodate sodu , Na 5 IO 6 można zsyntetyzować ze H 5 IO 6 .
Struktura
Kwas ortopejodowy tworzy kryształy jednoskośne ( grupa przestrzenna P2 1 / n ) składające się z lekko zdeformowanego oktaedru IO 6 połączonego mostkami wodorowymi. Pięć odległości wiązania I–O mieści się w zakresie 1,87–1,91 Å, a jedno wiązanie I–O wynosi 1,78 Å. Struktura kwasu metaperiodowego obejmuje również oktaedry IO 6 , jednak są one połączone poprzez współdzielenie krawędzi cis z tlenami mostkowymi, tworząc jednowymiarowe nieskończone łańcuchy.
Reakcje
Jak wszystkie nadjodany, kwas nadjodowy może być stosowany do rozszczepiania różnych związków 1,2-dwufunkcyjnych. Przede wszystkim kwas nadjodowy rozszczepi wicynalne diole na dwa fragmenty aldehydowe lub ketonowe ( reakcja Malaprade'a ).
Może to być przydatne w określaniu struktury węglowodanów, ponieważ kwas nadjodowy można stosować do otwierania pierścieni sacharydowych. Proces ten jest często stosowany w znakowaniu sacharydów cząsteczkami fluorescencyjnymi lub innymi znacznikami, takimi jak biotyna . Ponieważ proces wymaga dioli wicynalnych, utlenianie nadjodanem jest często stosowane do selektywnego znakowania 3'-końców RNA ( ryboza ma diole wicynalne ) zamiast DNA, ponieważ deoksyryboza nie ma dioli wicynalnych.
Kwas nadjodowy stosuje się również jako środek utleniający o umiarkowanej mocy, czego przykładem jest utlenianie Bablera drugorzędowych alkoholi allilowych, które są utleniane do enonów przez stechiometryczne ilości kwasu ortoperiodowego z katalizatorem PCC .
Inne kwasy tlenowe
Nadjodan jest częścią serii kwasów tlenowych, w których jod może przyjmować stopnie utlenienia -1, +1, +3, +5 lub +7. Znanych jest również wiele obojętnych tlenków jodu .
| Stan utlenienia jodu | -1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Nazwa | Jodek wodorowy | Kwas podjodowy | Kwas jodowy | Kwas jodowy | Kwas nadjodowy |
| Formuła | CZEŚĆ | HIO | HIO 2 | HIO 3 | HIO 4 lub H 5 IO 6 |
Zobacz też
Związki o podobnej strukturze:
- Kwas nadchlorowy , kwas perbromic i kwas perastatic , odpowiednie kwasy perhalogenic
- Kwas tellurowy i kwas nadksenowy , izoelektroniczne oxokwasy telluru i ksenonu
Związki o podobnej chemii: