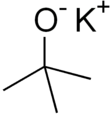Potasowy t -butoksylan -Potassium tert-butoxide
|
|
|||
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Potasowy t -butoksylan |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.011.583 |
||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 4 H 9 KO | |||
| Masa cząsteczkowa | 112,21 g mol- 1 | ||
| Wygląd | solidny | ||
| Temperatura topnienia | 256 ° C (493 ° F; 529 K) | ||
| Rozpuszczalność w eterze dietylowym | 4,34 g/100 g (25-26°C) | ||
| Rozpuszczalność w heksanie | 0,27 g/100 g (25-26°C) | ||
| Rozpuszczalność w toluenie | 2,27 g/100 g (25-26°C) | ||
| Rozpuszczalność w THF | 25,00 g/100 g (25-26°C) | ||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Karta charakterystyki dla Oksfordu | ||
|
Klasyfikacja UE (DSD) (nieaktualna)
|
Szkodliwy (Xn), Żrący (C) | ||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
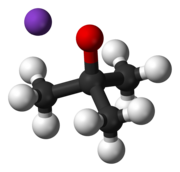
Potasowy t -butoksylan jest związek chemiczny o wzorze K + (CH 3 ) 3 CO - . Ta bezbarwna substancja stała jest silną zasadą (pKa sprzężonego kwasu około 17), która jest użyteczna w syntezie organicznej . Istnieje jako tetrameryczny klaster typu kubańskiego . Jest często postrzegany w literaturze chemicznej jako t -butanolan potasu. Związek jest często przedstawiany jako sól i często zachowuje się tak, ale nie jest zjonizowany w roztworze.
Przygotowanie
Potasowy t -butoksylan jest dostępny w handlu w postaci roztworu i w postaci substancji stałej, ale często jest generowany in situ do stosowania w laboratorium ponieważ próbki są tak wrażliwe i starsze próbki są często złej jakości. Otrzymuje się go w reakcji suchego alkoholu tert -butylowego z metalicznym potasem . Ciało stałe otrzymuje się przez odparowanie tych roztworów, a następnie ogrzewanie ciała stałego. Ciało stałe można oczyścić przez sublimację w 220 °C i 1 mmHg. Sublimacja może również zachodzić w 140 °C i 0,01 hPa. Wskazane jest przykrycie surowca wełną szklaną, ponieważ tert-butanolan potasu ma tendencję do „odbijania się”, więc części mogą być wyrzucane podczas sublimacji. Szczególnie korzystne jest usuwanie bezwodne za pomocą obojętnego aparatu sublimacyjnego.
Struktura
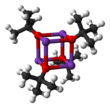
Potasowy t -butoksylan Wykrystalizowany z tetrahydrofuranu / pentanu w temperaturze -20 ° C jako [tBuOK · tBuOH] ∞ , który składa się z jednowymiarowego nieskończonych łańcuchów połączonych przez wiązania wodorowe . Sublimacja [tBuOK·tBuOH] ∞ daje tetramer [tBuOK] 4 , który przyjmuje strukturę zbliżoną do kubanu. Łagodne rozpuszczalniki zasadowe Lewisa, takie jak THF i eter dietylowy , nie rozbijają struktury tetramerycznej, która utrzymuje się w ciele stałym, w roztworze, a nawet w fazie gazowej.
Aplikacje
Sam związek tert -butanolanowy jest użyteczny jako silna, nienukleofilowa zasada w chemii organicznej. Nie jest tak mocny jak zasady amidowe, np. diizopropyloamidek litu , ale mocniejszy niż wodorotlenek potasu. Jego stearynowy luzem hamuje grupę udziału w addycji nukleofilowej, na przykład w Williamson eter syntezy lub S N 2 reakcji. Substraty deprotonowane przez t -butanolan potasu obejmują terminalne acetyleny i aktywne związki metylenowe . Jest przydatny w reakcjach dehydrohalogenacji .
Potasowy t -butoksylan katalizuje reakcję hydrosilanes i związków heterocyklicznych, z wytworzeniem pochodnych sililowych, z uwolnieniem H 2 .
Modyfikacje
Doniesiono o wielu modyfikacjach, które wpływają na reaktywność tego odczynnika. Związek przyjmuje złożoną strukturę klastrową (poniższy rysunek to uproszczony rysunek), a dodatki modyfikujące klaster wpływają na reaktywność odczynnika. Na przykład DMF , DMSO , heksametylofosforamid (HMPA) i 18-korona-6 oddziałują z centrum potasowym, wzmacniając zasadowość butoksydu. Zasada Schlossera , mieszanina alkoholanu i związku alkilolitu, jest pokrewną, ale silniejszą zasadą.
Reakcje
Potasu tert -butanolanu reaguje z chloroformu otrzymując dichlorocarbene , reakcję można prowadzić w zapłonu. Potasowy t -butoksylan nie powinny być dodawane do dichlorometanu.
Jako zasada, tert-butanolan potasu może ekstrahować beta-proton i tworzyć produkt Hofmanna poprzez reakcję eliminacji . Reakcja ta ma wysoką wartość syntetyczną, ponieważ może wywołać dalsze reakcje powstałego alkenu , zwłaszcza reakcje regiochemiczne.