Chlorek samaru (III) - Samarium(III) chloride

|
|
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
chlorek samaru (III)
|
|
| Inne nazwy
trichlorosamarium
trichlorku samaru |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.030.712 |
| Numer WE | |
|
PubChem CID
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| SmCl 3 | |
| Masa cząsteczkowa | 256,76 g / mol (bezwodna) 364,80 g / mol (heksa hydrat ) |
| Wygląd | bladożółte ciało stałe (bezwodne)
kremowe ciało stałe (heksahydrat) |
| Gęstość | 4,46 g / cm 3 (bezwodna)
2,383 g / cm 3 (heksahydrat) |
| Temperatura topnienia | 682 ° C (1260 ° F, 955 K) |
| Temperatura wrzenia | rozkłada się |
| 92,4 g / 100 ml (10 ° C ) | |
| Struktura | |
| sześciokątny , HP8 | |
| P6 3 / m, nr 176 | |
| Uwięziony trygonalny pryzmatyczny (dziewięć współrzędnych) |
|
| Zagrożenia | |
| Główne zagrożenia | Drażniący |
| Piktogramy GHS |

|
| Hasło ostrzegawcze GHS | Ostrzeżenie |
| H315 , H319 | |
| P264 , P280 , P302 + 352 , P305 + 351 + 338 , P321 , P332 + 313 , P337 + 313 , P362 | |
| Związki pokrewne | |
|
Inne aniony
|
Fluorek samaru (III) Bromek samaru (III) Tlenek samaru (III) |
|
Inne kationy
|
Chlorek samaru (II) Chlorek prometu (III) Chlorek europu (III) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Samaru (III) , znany również jako samar trójchlorek jest nieorganiczny związek w samaru i chlorku . Jest to blado żółta sól, która szybko absorbuje wodę z wytworzeniem heksa hydrat , SmCl 3 . 6H 2 O. Związek ma niewiele praktycznych zastosowań, ale jest używany w laboratoriach do badań nowych związków samaru.
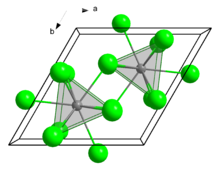
Struktura
Podobnie jak kilka pokrewnych chlorków lantanowców i aktynowców, SmCl 3 krystalizuje w motywie UCl 3 . Centra Sm 3+ są dziewięcioma współrzędnymi, zajmującymi trygonalne pryzmatyczne miejsca z dodatkowymi ligandami chlorkowymi zajmującymi trzy kwadratowe powierzchnie.
Przygotowanie i reakcje
SmCl 3 jest wytwarzany na drodze „ chlorku amonu ”, która obejmuje początkową syntezę (NH 4 ) 2 [SmCl 5 ]. Materiał ten można przygotować ze zwykłych materiałów wyjściowych w temperaturze reakcji 230 ° C z tlenku samaru :
- 10 NH 4 Cl + Sm 2 O 3 → 2 (NH 4 ) 2 [SmCl 5 ] + 6 NH 3 + 3 H 2 O
Pentachlorek jest następnie podgrzewany do 350-400 ° C, co powoduje wydzielanie się chlorku amonu i pozostawianie pozostałości bezwodnego trichlorku:
- (NH 4 ) 2 [SmCl 5 ] → 2NH 4 Cl + SmCl 3
Można go również przygotować z metalicznego samaru i kwasu solnego .
- 2 Sm + 6 HCl → 2 SmCl 3 + 3 H 2
Wodne roztwory chlorku samaru (III) można przygotować przez rozpuszczenie metalicznego samaru lub węglanu samaru w kwasie solnym .
Chlorek samaru (III) jest umiarkowanie mocnym kwasem Lewisa , który zgodnie z koncepcją HSAB klasyfikuje się jako „twardy” . Do przygotowania trifluorku samaru można użyć wodnych roztworów chlorku samaru :
- SmCl 3 + 3 KF → SmF 3 + 3 KCl
Używa
Chlorek samaru (III) jest używany do wytwarzania metalu samaru , który ma różne zastosowania, zwłaszcza w magnesach . Bezwodny SmCl 3 miesza się z chlorku sodu i chlorku wapnia z wytworzeniem LOW Temperatura topnienia mieszaniny eutektycznej. Elektroliza tego stopionego roztworu soli daje wolny metal .
W laboratorium
Chlorek samaru (III) może być również użyty jako punkt wyjścia do przygotowania innych soli samaru . Bezwodny chlorek służy do otrzymywania metaloorganicznych związków samaru, takich jak kompleksy bis (pentametylocyklopentadienylo) alkilosamarium (III).
