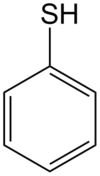
Tiofenol - Thiophenol
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Benzenetiol |
|||
| Inne nazwy | |||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.003.306 |
||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 6 H 6 S | |||
| Masa cząsteczkowa | 110,17 g·mol -1 | ||
| Wygląd zewnętrzny | Bezbarwna ciecz | ||
| Zapach | Nieprzyjemny, cierpki | ||
| Gęstość | 1,0766 g/ml | ||
| Temperatura topnienia | -15 ° C (5 ° F; 258 K) | ||
| Temperatura wrzenia | 169 ° C (336 ° F; 442 K) | ||
| 0,08% | |||
| Rozpuszczalność | Większość rozpuszczalników organicznych; wodna baza | ||
| Ciśnienie pary | 1 mmHg (18°C) | ||
| Kwasowość (p K a ) | |||
| -70,8 x 10 -6 cm 3 / mol | |||
| Zagrożenia | |||
| Główne zagrożenia | Toksyczny | ||
| Zwroty R (nieaktualne) | R10 R24/25 R26 R41 | ||
| Zwroty S (nieaktualne) | S23 S26 S28 S36/37/39 S45 | ||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | 56°C; 132 ° F; 329 tys | ||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
Żaden | ||
|
REL (zalecane)
|
C 0,1 ppm (0,5 mg/m 3 ) [15 minut] | ||
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
NS | ||
| Związki pokrewne | |||
|
Powiązane tiole
|
1,2-Benzenedithiol Benzenemethanethiol |
||
|
Związki pokrewne
|
Fenol Benzeneselenol Dwusiarczek difenylu |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Tiofenolu jest związek siarkoorganiczne o wzorze C 6 H 5 SH, czasami w skrócie PhSH. Ta śmierdząca bezbarwna ciecz jest najprostszym aromatycznym tiolem . Struktury chemiczne tiofenolu i jego pochodnych są analogiczne do fenoli z tym wyjątkiem, że atom tlenu w grupie hydroksylowej (-OH) związany z pierścieniem aromatycznym jest zastąpiony atomem siarki . Przedrostek tio- oznacza związek zawierający siarkę, a użyty przed nazwą rdzenia nazwy związku, który normalnie zawierałby atom tlenu, w przypadku „tiolu” oznacza to, że atom tlenu alkoholu jest zastąpiony atomem siarki.
Tiofenole opisują również klasę związków formalnie pochodzących od samego tiofenolu. Wszystkie mają grupę sulfhydrylową (-SH) kowalencyjnie związaną z pierścieniem aromatycznym. Ligandem siarkoorganicznym w medycynie tiomersalu jest tiofenol.
Synteza
Istnieje kilka metod syntezy tiofenolu i związków pokrewnych, chociaż sam tiofenol jest zwykle kupowany do operacji laboratoryjnych. Sposoby obejmują redukcję chlorku benzenosulfonylu z cynkiem . oraz działanie siarki elementarnej na halogenek fenylomagnezowy lub fenylolit, a następnie zakwaszenie.
Poprzez przegrupowanie Newmana-Kwarta fenole ( 1 ) mogą być przekształcone w tiofenole ( 5 ) przez konwersję do O-arylu dialkilotiokarbaminianów ( 3 ), a następnie przez ogrzewanie z wytworzeniem izomerycznej pochodnej S -arylowej ( 4 ).
W Leuckart tiofenolu reakcji materiał wyjściowy jest anilina przez sól dwuazoniową (ARN 2 X) i ksantogenian (ArS (C = S)). Alternatywnie, siarczek sodu i triazen mogą reagować w roztworach organicznych i dawać tiofenole.
Tiofenol można wytwarzać z chlorobenzenu i siarkowodoru na tlenku glinu w temperaturze od 700 do 1300 ° F (371 do 704 ° C). Dwusiarczek jest głównym produktem ubocznym. Medium reakcyjne jest korozyjne i wymaga ceramicznej lub podobnej wykładziny reaktora. Jodki arylu i siarka w pewnych warunkach mogą również wytwarzać tiofenole.
Aplikacje
Tiofenole wykorzystywane są do produkcji farmaceutyków, w tym sulfonamidów . Środki przeciwgrzybicze butokonazol i mertiolan są pochodnymi tiofenoli.
Właściwości i reakcje
Kwasowość
Tiofenolu ma znacznie większą kwasowość niż sama fenolu, jak wykazano na podstawie ich P K a wartości (6,62 do tiofenolu i 9,95 do fenolu). Podobny wzór widać na H 2 S w stosunku H 2 O i wszystkie tioli w porównaniu z odpowiednimi alkoholami . Traktowanie PhSH mocną zasadą, taką jak wodorotlenek sodu (NaOH) lub metaliczny sód daje sól tiofenolan sodu (PhSNa).
Alkilacja
Tiofenolan jest wysoce nukleofilowy, co przekłada się na wysoki stopień alkilacji. Zatem, traktowanie grupy C 6 H 5 SH się jodek metylu w obecności zasady daje metylofenylo siarczek C 6 H 5 SCH 3 , A tioeter często nazywane tioanizol . Takie reakcje są dość nieodwracalne. C 6 H 5 SH dodaje również a, P-nienasyconych karbonylki przez addycję Michaela .
Utlenianie
Tiofenole, szczególnie w obecności zasady, łatwo utleniają się do dwusiarczku difenylu :
- 4 C 6 H 5 SH + O 2 → 2 C 6 H 5 S-SC 6 H 5 + 2 H 2 O
Dwusiarczek można zredukować z powrotem do tiolu stosując borowodorek sodu, a następnie zakwasić. Ta reakcja redoks jest również wykorzystywana przy użyciu C 6 H 5 SH jako źródła atomów H.
Chlorowanie
Chlorek fenylosulfenylu, krwistoczerwony płyn (temperatura wrzenia 41–42 °C, 1,5 mm Hg), można wytworzyć w reakcji tiofenolu z chlorem (Cl 2 ).
Koordynacja do metali
Kationy metali tworzą tiofenolany, z których niektóre są polimerami. Jednym z przykładów jest „C 6 H 5 scu” otrzymuje się przez działanie chlorku miedzi (I) z tiofenolem.
Bezpieczeństwo
Amerykański Narodowy Instytut Bezpieczeństwa i Higieny Pracy ustalił zalecany limit narażenia na pułap 0,1 ppm (0,5 mg m- 3 ) i narażenia nie dłuższe niż 15 minut.
Bibliografia
- ^ „Przód Materia” . Nomenklatura chemii organicznej: zalecenia IUPAC i preferowane nazwy 2013 (Blue Book) . Cambridge: Królewskie Towarzystwo Chemiczne . 2014. s. P001–P004. doi : 10.1039/9781849733069-FP001 . Numer ISBN 978-0-85404-182-4.
- ^ a b c d e f Kieszonkowy przewodnik po zagrożeniach chemicznych NIOSH. „#0050” . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ Cox, Brian G. Kwasy i zasady: Wpływ rozpuszczalnika na siłę kwasowo-zasadową. 1 wyd. Oksford, Wielka Brytania: Oxford UP, 2013.
- ^ Bordwell, Fryderyk G.; Hughes, David L. (1982). „Kwasowości tiolowe i reaktywności tiolanowe wobec chlorku butylu w roztworze dimetylosulfotlenku. Kwestia krzywizny w wykresach Broensteda”. Czasopismo Chemii Organicznej . 47 (17): 3224–3232. doi : 10.1021/jo00138a005 .
- ^ Adams, R.; CS Marvel, CS „Tiofenol” . Syntezy organiczne .CS1 maint: wiele nazwisk: lista autorów ( link ); Tom zbiorowy , 1 , s. 504.
- ^ Melvin S. Newman i Frederick W. Hetzel (1971). „Tiofenole z fenoli: 2-naftalenotiol”. Syntezy organiczne . 51 : 139. doi : 10.15227/orgsyn.051.0139 .
- ^ Leuckart , J. Prakt. Chem. , [2] 41, 189 ( 1890 ).
- ^ Tarbell, DS; Fukushima, DK (1947). „ m- tiokrezol” . Syntezy organiczne . 27 : 81. doi : 10.15227/orgsyn.027.0081 .; Tom zbiorowy , 3 , s. 809
- ^ B Kazem-Rostami, Masoud; Khazaei, Ardeshir; Moosavi-Zare, Ahmad; Bajat, Mahomet; Saednia, Szahnaz (2012). „Synteza jednogarnkowa tiofenoli”. Synletta . 23 (13): 1893-1896. doi : 10.1055/s-0032-1316557 .
- ^ Patent US 2,490,257 , Duncan J. Crowley i Alvin L Kosak, „Mono- and Polyalkil Mono- and Polynuclear Mercaptans”, wydany 1949-12-06, przypisany do Socony-Vacuum Oil Co.
- ^ Jiang, Y.; Qin, Y.; Xie, S.; Zhang, X.; Dong, J.; Ma, D., A (2009). „Ogólne i skuteczne podejście do arylowych tioli: sprzęganie katalizowane CuI z jodkami arylu z siarką i późniejszą redukcją”. Litery organiczne . 22 (1): 52–56. doi : 10.1021/acs.orglett.9b03866 . PMID 31833778 .CS1 maint: wiele nazwisk: lista autorów ( link )
- ^ Campopiano, O. (2004). „Tiofenol”. Encyklopedia odczynników do syntezy organicznej . Nowy Jork: John Wiley i Synowie . doi : 10.1002/047084289X . hdl : 10261/236866 . Numer ISBN 9780471936237..
- ^ Barrett, ZWZ; Dhanak, D.; Graboski, GG; Taylor SJ (1993). „(Fenylotio)nitrometan” . Syntezy organiczne .CS1 maint: wiele nazwisk: lista autorów ( link ); Tom zbiorowy , 8 , s. 550
- ^ Posner, GH; Whitten, CE "drugorzędowe i trzeciorzędowe ketony alkilowe z chlorków kwasów karboksylowych i odczynniki litowo-fenylotio(alkilo)miedzianowe: tert - butylofenyloketon " . Syntezy organiczne .CS1 maint: wiele nazwisk: lista autorów ( link ); Tom zbiorowy , 6 , s. 248
- ^ CDC - NIOSH kieszonkowy przewodnik po zagrożeniach chemicznych
Zewnętrzne linki
- Tiofenol , sieć danych toksykologicznych