Ylide - Ylide
Ylid lub ylidem ( / ɪ l ɪ d / ) jest obojętny dipolarny cząsteczki zawierające formalnie ujemnie naładowanego atomu (zazwyczaj karboanionowych ), bezpośrednio związaną z heteroatomem z formalny ładunek dodatni (zazwyczaj azotu, fosforu i siarki), i gdzie oba atomy mają pełne oktety elektronów. Wynik można postrzegać jako strukturę, w której dwa sąsiednie atomy są połączone wiązaniem kowalencyjnym i jonowym ; normalnie napisane X + –Y - . Ylidy są zatem związkami 1,2- dipolarnymi i podklasą jonów obojnaczych . Występują w chemii organicznej jako odczynniki lub reaktywne półprodukty .
Nazwa klasy „ylide” dla związku nie powinna być mylona z przyrostkiem „-ylide”.
Struktury rezonansowe
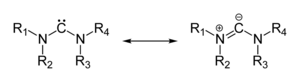
Wiele ylidów można zobrazować za pomocą wielu form wiązań w strukturze rezonansowej , znanej jako forma ylenu, podczas gdy rzeczywista struktura leży pomiędzy obiema formami:
Rzeczywisty obraz wiązania tego typu ylidów jest ściśle obojnaczojonowy (struktura po prawej) z silnym przyciąganiem kulombowskim między atomem „onu” a sąsiednim węglem odpowiadającym za zmniejszoną długość wiązania. W konsekwencji anion węgla jest piramidą trygonalną.
Ylidy fosfoniowe
 Struktura metylenu trifenylo-fosforanem .
Struktura metylenu trifenylo-fosforanem .
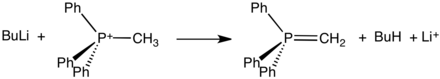
W reakcji Wittiga , metodzie stosowanej do konwersji ketonów, a zwłaszcza aldehydów, do alkenów stosuje się ylidy fosfoniowe . Dodatni ładunek w tych odczynnikach Wittiga jest przenoszony przez atom fosforu z trzema podstawnikami fenylowymi i wiązaniem z karboanionem . Ylidy mogą być „stabilizowane” lub „niestabilizowane”. Ylid fosfoniowy można wytworzyć dość prosto. Zazwyczaj trifenylofosfina reaguje z halogenkiem alkilu w mechanizmie analogicznym do reakcji S N2 . To czwartorzędowanie tworzy alkyltriphenyl fosfoniową sól, która może być wyizolowana lub traktuje się in situ z mocną zasadą (w tym przypadku, butylolit ) z wytworzeniem ylidu.
Ze względu na mechanizm S N2 , halogenek alkilu z mniejszą zawadą przestrzenną reaguje korzystniej z trifenylofosfiną niż halogenek alkilu ze znaczną zawadą przestrzenną (taki jak bromek tert-butylu ). Z tego powodu w syntezie z udziałem takich związków zazwyczaj będzie istniała jedna droga syntezy, która jest korzystniejsza niż inna.
Ylidy fosforu są ważnymi odczynnikami w chemii organicznej, zwłaszcza w syntezie naturalnie występujących produktów o działaniu biologicznym i farmakologicznym. Duże zainteresowanie właściwościami koordynacyjnymi a-keto stabilizowanych ylidów fosforowych wynika z ich wszechstronności koordynacyjnej, wynikającej z obecności różnych grup funkcyjnych w ich strukturze molekularnej.
Niesymetryczne ylidy fosforowe
Stabilizowane a-keto ylidy pochodzące od bisfosfin, takich jak dppe , dppm , itp., A mianowicie [Ph 2 PCH 2 PPh 2 ] C (H) C (O) R i [Ph 2 PCH 2 CH 2 PPh 2 ] C ( H) C (O) R (R = Me, Ph lub OMe) stanowią ważną klasę ligandów hybrydowych zawierających zarówno funkcje fosfinowe , jak i ylidowe i mogą występować w formach ylidowych i enolanowych. Dlatego te ligandy mogą być zaangażowane w różnego rodzaju wiązania z jonami metali, takimi jak pallad i platyna .
Inne rodzaje
Na bazie siarki
Inne popularne ylidy obejmują ylidy sulfoniowe i ylidy sulfoksoniowe , na przykład odczynnik Corey-Chaykovsky'ego stosowany do wytwarzania epoksydów lub w przegrupowaniu Stevensa .
Na bazie tlenu
Ylidy karbonylowe (RR'C = O + C - RR ') mogą tworzyć się przez otwarcie pierścienia epoksydów lub przez reakcję karbonylków z elektrofilowymi karbenami , które zwykle wytwarza się ze związków diazowych . Ylidy oksoniowe (RR'-O + -C - R'R) powstają w wyniku reakcji eterów z elektrofilowymi karbenami .
Na bazie azotu
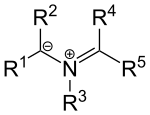
Istnieją również pewne ylidy na bazie azotu , takie jak ylidy azometynowe o ogólnej strukturze:
Związki te można sobie wyobrazić jako kationy iminiowe umieszczone obok karboanionu . Te podstawniki R 1 , R 2 są grupy odciągające elektron . Te ylidy można wytworzyć przez kondensację α- aminokwasu i aldehydu lub przez reakcję termicznego otwarcia pierścienia pewnych N-podstawionych azyrydyn .
Dość egzotyczną rodziną ylidów na bazie diazotu są izodiazeny : R 1 R 2 N + = N - . Generalnie rozkładają się przez wytłaczanie diazotu.
Stabilne karbeny mają również udział w rezonansie ylidowym, np .:
Inny
Ylidy haloniowe można wytwarzać z halogenków allilu i karbenoidów metali . Po przegrupowaniu [2,3] - otrzymuje się halogenek homoallilu.
Aktywna postać odczynnika Tebbe jest często uważana za ylid tytanowy. Podobnie jak odczynnik Wittiga, jest w stanie zastąpić atom tlenu w grupach karbonylowych grupą metylenową. W porównaniu z odczynnikiem Wittiga ma większą tolerancję na grupy funkcyjne.
Reakcje
Ważną reakcją ylidową jest oczywiście reakcja Wittiga (dla fosforu), ale jest ich więcej.
Dipolarne cykloaddycje
Niektóre ylidy są 1,3-dipolami i oddziałują w 1,3-dipolarnych cykloaddycjach . Na przykład ylid azometynowy jest dipolem w reakcji Prato z fulerenami .
Dehydrosprzęganie z silanami
W obecności katalizatora homoleptycznego grupy 3 Y [N (SiMe 3 ) 2 ] 3 metylid trifenylofosfoniowy można sprzęgać z fenylosilanem . Reakcja ta H 2 gazu przez produkt i tworzy sililową stabilizowany ylidu.
Przegrupowania sigmatropowe
Wiele ylidów reaguje w reakcjach sigmatropowych . Sommelet-Hauser przegrupowanie jest przykładem [2,3] -sigmatropic reakcji. Stevensa przegrupowania oznacza grupę [1,2] -rearrangement.
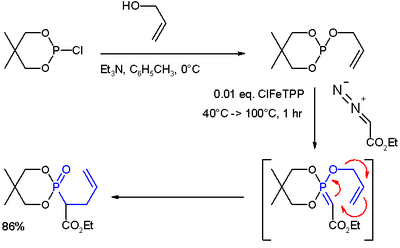
W niektórych ylidach fosfoniowych obserwowano reakcję [3,3] -sigmatropową
Sojusznicze przegrupowania
Stwierdzono, że odczynniki Wittiga reagują jako nukleofile w substytucji SN 2 ' :
Po początkowej reakcji addycji następuje reakcja eliminacji .
Zobacz też
- 1,3-dipol
- Betaina : neutralna cząsteczka z kationem onowym i ładunkiem ujemnym
- Zwitterion : neutralna cząsteczka z jedną lub więcej parami ładunków dodatnich i ujemnych