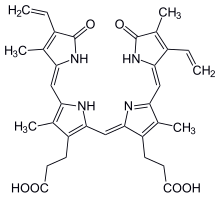
Biliverdin - Biliverdin
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
3,3 ′ - (2,17-dietenylo-3,7,13,18-tetrametylo-1,19-diokso-19,21,22,24-tetrahydro-1 H -bilino-8,12-diylo) dipropan kwas
|
|
|
Preferowana nazwa IUPAC
3,3 ′ - ([1 2 (2) Z , 4 (5 2 ) Z , 6 (7 2 ) Z ] -1 3 , 7 4 -Dietenylo-1 4 , 3 3 , 5 4 , 7 3- tetrametyl -1 5 , 7 5 -diokso-1 1 , 1 5 , 7 1 , 7 5 -tetrahydro-3 1 H -1,7 (2), 3,5 (2,5) -tetrapiroloheptafan-1 2 (2) Kwas 4 (5 2 ), 6 (7 2 ) -trieno-3 4 , 5 3 -diylo) dipropanowy |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA |
100,003,675 |
| Siatka | Biliverdin |
|
PubChem CID
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 33 H 34 N 4 O 6 | |
| Masa cząsteczkowa | 582,646 |
| Temperatura topnienia | > 300 ° C |
| Zagrożenia | |
| Główne zagrożenia | Drażniący |
| Arkusz danych dotyczących bezpieczeństwa | Sigma-Aldrich |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Biliverdin to zielony tetrapiroliczny pigment żółci , będący produktem katabolizmu hemu . Jest to pigment odpowiedzialny za zielonkawy kolor, czasami widoczny na siniakach .
Metabolizm
Biliverdin powstaje w wyniku rozpadu ugrupowania hemu hemoglobiny w erytrocytach . Makrofagi rozkładają starzejące się erytrocyty i rozkładają hem na biliwerdynę wraz z hemosyderyną , w której biliwerdyna normalnie szybko redukuje się do wolnej bilirubiny .
Biliverdin jest przez chwilę widoczny w niektórych siniakach jako zielony kolor. W siniakach jego rozpad na bilirubinę prowadzi do żółtawego koloru.
Rola w chorobie
Biliverdin wykryto w nadmiarze we krwi ludzi cierpiących na choroby wątroby. Żółtaczka jest spowodowana nagromadzeniem biliwerdyny lub bilirubiny (lub obu) w układzie krążenia i tkankach. Żółtaczka i twardówka (białka oczu) są charakterystyczne dla niewydolności wątroby.
Rola w leczeniu chorób
Chociaż zwykle uważany za zwykły produkt odpadowy rozkładu hemu, rośnie liczba dowodów, które sugerują, że biliwerdyna - i inne pigmenty żółciowe - odgrywa fizjologiczną rolę u ludzi.
Pigmenty żółciowe, takie jak biliwerdyna, mają znaczące właściwości przeciwmutagenne i przeciwutleniające, a zatem mogą pełnić pożyteczną funkcję fizjologiczną. Wykazano, że biliwerdyna i bilirubina są silnymi zmiataczami rodników hydroperoksylowych . Wykazano również, że hamują one działanie policyklicznych węglowodorów aromatycznych , amin heterocyklicznych i utleniaczy - z których wszystkie są mutagenami . Niektóre badania wykazały, że osoby z wyższym stężeniem bilirubiny i biliwerdyny w organizmie mają mniejszą częstość występowania raka i chorób układu krążenia . Sugerowano, że biliwerdyna - podobnie jak wiele innych pigmentów tetrapirolicznych - może działać jako inhibitor proteazy HIV-1 , a także mieć korzystny wpływ na astmę, chociaż potrzebne są dalsze badania, aby potwierdzić te wyniki. Obecnie nie ma praktycznych implikacji stosowania leku Biliverdin w leczeniu jakiejkolwiek choroby.
U zwierząt innych niż ludzie
Biliverdin jest ważnym składnikiem pigmentu w skorupkach jaj ptasich , zwłaszcza w niebieskich i zielonych skorupkach. Niebieskie skorupki jaj mają znacznie wyższe stężenie biliwerdyny niż brązowe skorupki jaj.
Badania wykazały, że biliwerdyna skorupek jaj jest wytwarzana z gruczołu muszli, a nie z rozpadu erytrocytów w krwiobiegu, chociaż nie ma dowodów, że źródłem tego materiału nie są ani tetrapirole, ani wolny hem z osocza krwi.
Oprócz jej obecności w skorupkach jaj ptasich, inne badania wykazały również, że biliverdin jest obecny w niebieskozielonej krwi wielu ryb morskich, krwi rogówki tytoniowej , skrzydłach ćmy i motyla, surowicy i jajach żab oraz łożysko psów. W przypadku psów może to w niezwykle rzadkich przypadkach prowadzić do narodzin szczeniąt z zielonym futrem; jednak zielony kolor zanika wkrótce po urodzeniu. U belony ( Belone belone ) i gatunków pokrewnych, kości są jasnozielone z powodu biliverdin.
Biliwerdyna jest również obecny w zielonej krwi, mięśnie, kości i śluzówki wyściółka Scynki z rodzaju Prasinohaema , znajdujące się w Nowej Gwinei . Nie jest pewne, czy ta obecność biliwerdyny jest jakąkolwiek adaptacją ekologiczną lub fizjologiczną. Sugerowano, że kumulacja biliwerdyny może powstrzymać szkodliwe zakażenie pasożytami malarii Plasmodium , chociaż nie ustalono statystycznie istotnej korelacji. Cechę tę wykazuje również żaba kambodżańska Chiromantis samkosensis wraz z turkusowymi kośćmi.
W obrazowaniu fluorescencyjnym

W kompleksie ze zmodyfikowanym fitochromem bakteryjnym biliwerdyna została wykorzystana jako chromofor emitujący promieniowanie podczerwone do obrazowania in vivo. W przeciwieństwie do białka fluorescencyjne , które tworzą ich chromofor przez potranslacyjne modyfikacje w łańcuchu polipeptydowym , fitochromów wiązania zewnętrznego ligandu (w tym przypadku, biliwerdyny) oraz skutecznego zobrazowania pierwszej sondy bacteriophytochrome oparte wymaga dodawania egzogennego biliwerdyny. Niedawne badania wykazały, że białka fluorescencyjne oparte na bakteriofitochromach o wysokim powinowactwie do biliwerdyny mogą być obrazowane in vivo z wykorzystaniem tylko endogennego ligandu, a zatem z taką samą łatwością jak konwencjonalne białka fluorescencyjne. Pojawienie się drugiej i kolejnych generacji sond opartych na bakteriofitochromach wiążących biliwerdynę powinno poszerzyć możliwości nieinwazyjnego obrazowania in vivo.
Nowa klasa białka fluorescencyjnego została wyewoluowana z fikobiliproteiny cyjanobakteryjnej ( Trichodesmium erythraeum ) , α- allofikocyjaniny i nazwanej małym ultra czerwonym białkiem fluorescencyjnym ( smURFP ) w 2016 r. SmURFP autokatalitycznie wbudowuje chromofor biliverdin bez potrzeby stosowania zewnętrznego białka , znany jako liaza . Meduza - i białka fluorescencyjne pochodzące z koralowców wymagają tlenu i wytwarzają stechiometryczną ilość nadtlenku wodoru podczas tworzenia chromoforów . smURFP nie wymaga tlenu ani nie wytwarza nadtlenku wodoru i wykorzystuje chromofor biliverdin. smURFP ma duży współczynnik ekstynkcji (180 000 M −1 cm –1 ) i ma niewielką wydajność kwantową (0,20), co czyni go porównywalnym biofizyczną jasnością do eGFP i ~ 2-krotnie jaśniejszą niż większość czerwonych lub dalekiej czerwieni fluorescencyjnych białek pochodzących z koral . Właściwości widmowe smURFP są podobne do organicznego barwnika Cy5 .

