Tribromek boru - Boron tribromide
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Tribromek boru
|
|
| Inne nazwy
Tribromoboran, bromek boru
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.030.585 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 2692 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| B Br 3 | |
| Masa cząsteczkowa | 250,52 g·mol -1 |
| Wygląd | Bezbarwna lub bursztynowa ciecz |
| Zapach | Ostre i irytujące |
| Gęstość | 2,643 g/cm 3 |
| Temperatura topnienia | -46,3 ° C (-51,3 ° F; 226,8 K) |
| Temperatura wrzenia | 91,3 ° C (196,3 ° F; 364,4 K) |
| Reaguje gwałtownie z wodą i innymi rozpuszczalnikami protonowymi | |
| Rozpuszczalność | Rozpuszczalny w CH 2 Cl 2 , CCl 4 |
| Ciśnienie pary | 7,2 kPa (20 °C) |
|
Współczynnik załamania ( n D )
|
1.00207 |
| Lepkość | 7,31 x 10-4 Pa·s (20 °C) |
| Termochemia | |
|
Pojemność cieplna ( C )
|
0,2706 J/K |
|
Standardowa
entropia molowa ( S |
228 J/mol K |
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-0,8207 kJ/g |
| Zagrożenia | |
| Główne zagrożenia | Reaguje gwałtownie z wodą, potasem, sodem i alkoholami; atakuje metale, drewno i gumę |
| Arkusz danych dotyczących bezpieczeństwa | ICSC 0230 |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Niebezpieczeństwo |
| H330 , H300 , H314 W Unii Europejskiej na etykiecie należy również umieścić następujący dodatkowy zwrot wskazujący rodzaj zagrożenia (EUH014): Reaguje gwałtownie z wodą. | |
| NFPA 704 (ognisty diament) | |
| Temperatura zapłonu | Niepalny |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
Żaden |
|
REL (zalecane)
|
C 1 ppm (10 mg/m 3 ) |
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
ND |
| Związki pokrewne | |
|
Związki pokrewne
|
Trifluorek boru Trichlorek boru Trijodek boru |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
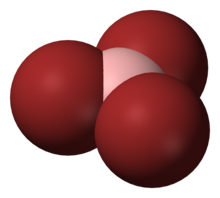
Tribromek boru BBr 3 jest bezbarwnym, dymiącym ciekłym związkiem zawierającym bor i brom . Próbki handlowe zwykle mają barwę bursztynową do czerwonej/brązowej ze względu na słabe zanieczyszczenie bromem. Rozkłada się pod wpływem wody i alkoholi.
Właściwości chemiczne
Tribromek boru jest dostępny w handlu i jest silnym kwasem Lewisa .
Jest to doskonały demetylowanie lub środek dealkilując do rozszczepiania z eterów , również następnie cyklizacji, często w produkcji leków .
Mechanizm dealkilacji trzeciorzędowych eterów alkilowych przebiega poprzez tworzenie kompleksu między centrum boru a tlenem eterowym, a następnie eliminację bromku alkilu z wytworzeniem dibromo(organo) boranu .
- ROR + BBr 3 → RO + ( − BBr 3 )R → ROBBr 2 + RBr
Eterów metylowo-arylowych (jak również etery alkilowe aktywowane pierwotne), z drugiej strony są dealkilowanych przez dwucząsteczkowej mechanizmu z udziałem dwóch BBR 3 -eteru adduktów.
- RO + ( − BBr 3 ) CH 3 + RO + ( − BBr 3 )CH 3 → RO( − BBr 3 ) + CH 3 Br + RO + (BBr 2 )CH 3
Dibromo(organo)boran może następnie ulegać hydrolizie, dając jako produkty grupę hydroksylową, kwas borowy i bromowodór .
- ROBBr 2 + 3 H 2 O → ROH + B (OH) 3 + 2HBr
Znajduje również zastosowanie w polimeryzacji olefin oraz w chemii Friedel-Crafts jako katalizator kwasowy Lewisa .
Przemysł elektroniczny wykorzystuje tribromek boru jako źródło boru w procesach osadzania wstępnego w celu domieszkowania w produkcji półprzewodników . Dodano tribromek boru pośredniczy również dealkilacji aryl etery alkilowe, na przykład demetylację z 3,4-dimethoxystyrene w 3,4-dihydroxystyrene .
Synteza
Reakcja węglika boru z bromem w temperaturach powyżej 300°C prowadzi do powstania trójbromku boru. Produkt można oczyścić metodą destylacji próżniowej .
Historia
Pierwszą syntezę wykonał Poggiale w 1846 roku, poddając reakcji trójtlenek boru z węglem i bromem w wysokich temperaturach:
- B 2 O 3 + 3 C + 3 Br 2 → 2 BBr 3 + 3 CO
Udoskonalenie tej metody zostało opracowane przez F. Wöhlera i Deville'a w 1857 roku. Wychodząc od amorficznego boru temperatury reakcji są niższe i nie powstaje tlenek węgla:
- 2 b + 3Br 2 → 2 BBR 3
Aplikacje
Tribromek boru jest stosowany w syntezie organicznej, produkcji farmaceutycznej, przetwarzaniu obrazu, domieszkowaniu półprzewodników, trawieniu plazmowym półprzewodników i produkcji fotowoltaicznej.
Zobacz też
Bibliografia
Dalsza lektura
- Doyagüez, EG (2005). „Trójbromek boru” (PDF) . Synletta . 2005 (10): 1636-1637. doi : 10.1055/s-2005-868513 . Zarchiwizowane z oryginału (pdf) w dniu 2014-12-07 . Źródło 16.05.2012 .
Linki zewnętrzne
- Tribromku boru w układzie okresowym filmów (University of Nottingham)
- Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych - Tribromek boru (Centra Kontroli i Zapobiegania Chorobom)
- „Karta Charakterystyki – Tribromek boru” . Nauka rybaka.
- patent USA 2989375 , May, FH; Bradford, JL, "Production of Boron Tribromide", wydany 20.06.1961, przypisany do American Potash & Chemical

