Tiofen - Thiophene
|
|
|||
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
Tiofen |
|||
| Inne nazwy
Tiofuranu
Thiacyclopentadiene tiolu |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100,003,392 |
||
|
PubChem CID
|
|||
| Numer RTECS | |||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 4 H 4 S | |||
| Masa cząsteczkowa | 84,14 g / mol | ||
| Wygląd | bezbarwna ciecz | ||
| Gęstość | 1,051 g / ml cieczy | ||
| Temperatura topnienia | -38 ° C (-36 ° F; 235 K) | ||
| Temperatura wrzenia | 84 ° C (183 ° F, 357 K) | ||
| -57,38 · 10-6 cm 3 / mol | |||
|
Współczynnik załamania ( n D )
|
1.5287 | ||
| Lepkość | 0,8712 c P przy 0,2 ° C 0,6432 c P przy 22,4 ° C |
||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna Karta Charakterystyki , Zewnętrzna Karta Charakterystyki | ||
|
Klasyfikacja UE (DSD) (nieaktualne)
|
nie wymienione | ||
| NFPA 704 (ognisty diament) | |||
| Temperatura zapłonu | −1 ° C (30 ° F, 272 K) | ||
| Związki pokrewne | |||
|
Powiązane tioetery
|
Tetrahydrotiofen Siarczek dietylu |
||
|
Związki pokrewne
|
Furan Selenophene Pirol |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencje Infobox | |||
Tiofen jest związkiem heterocyklicznym o wzorze C 4 H 4 S. Składający się z płaskiego pięcioczłonowego pierścienia jest aromatyczny, na co wskazują jego rozległe reakcje podstawienia . Jest to bezbarwna ciecz o zapachu przypominającym benzen . W większości reakcji przypomina benzen . Analogiczne związki tiofen obejmują furanu (C 4 H 4 O) selenophene (C 4 H 4 Se) i pirolu (C 4 H 4 NH), które różnią się od siebie na heteroatomie w pierścieniu.
Izolacja i występowanie
Tiofen został odkryty jako zanieczyszczenie benzenu. Zaobserwowano, że izatyna ( indol ) tworzy niebieski barwnik po zmieszaniu jej z kwasem siarkowym i surowym benzenem. Od dawna uważano, że powstanie niebieskiej indofeniny jest reakcją samego benzenu. Viktorowi Meyerowi udało się wyodrębnić tiofen jako właściwą substancję odpowiedzialną za tę reakcję.
Tiofen, a zwłaszcza jego pochodne, występują w ropie naftowej , czasami w stężeniach do 1–3%. Zawartość tiofenów w oleju i węglu jest usuwana w procesie hydroodsiarczania (HDS). W HDS wsad ciekły lub gazowy przepuszcza się w postaci dwusiarczku molibdenu katalizatora pod ciśnieniem H 2 . Tiofeny ulegają hydrogenolizie z wytworzeniem węglowodorów i siarkowodoru . Tak więc, tiofen sam przekształca się w butan i H 2 S. Bardziej rozpowszechnione bardziej problematyczne naftowego benzotiofen i dibenzotiofen .
Na Marsie
Pochodne tiofenu wykryto na poziomie nanomoli w marsjańskich osadach glebowych sprzed 3,5 miliarda lat (formacja Murray, Pahrump Hills) przez łazik Curiosity w kraterze Gale (Mars) w latach 2012–2017. Stanowi to ważny kamień milowy dla misji Mars Science. Laboratorium (MSL) w długich i nieuchwytnych poszukiwaniach materii organicznej na Czerwonej Planecie. Ogrzewanie w wysokiej temperaturze (od 500 ° do 820 ° C) próbek mułowca jeziornego za pomocą instrumentu Sample Analysis at Mars (SAM) umożliwiło analizę wydzielonych gazów metodą chromatografii gazowej i spektrometrii mas ( GC-MS ) oraz wykrywanie cząsteczek aromatycznych i alifatycznych w tym kilka związków tiofenowych. Obecność wiązań węgiel-siarka w makrocząsteczkach mogła przyczynić się do zachowania materii organicznej w bardzo długim okresie. Szacuje się, że ~ 5% cząsteczek organicznych analizowanych przez instrument SAM zawiera siarkę organiczną. Pochodzenie i sposób powstawania tych cząsteczek jest nadal nieznany, czy to biotyczny, czy abiotyczny , ale ich odkrycie postawiło zagadkową kwestię związków tiofenowych jako możliwej starożytnej biosygnatury na Marsie. Szczegółowe analizy izotopów węgla (δ 13 C) na poziomie śladowym przez następną generację łazików marsjańskich, takich jak Rosalind Franklin , będą konieczne, aby określić, czy takie cząsteczki organiczne są wzbogacone w lekki węgiel ( 12 C), jak zwykle żywe mikroorganizmy są na Ziemi.
Synteza i produkcja
Odzwierciedlając ich wysoką stabilność, tiofeny powstają w wyniku wielu reakcji z udziałem źródeł siarki i węglowodorów, zwłaszcza nienasyconych. Pierwsza synteza tiofenu przez Meyera, opisana w tym samym roku, w którym dokonał swojego odkrycia, obejmuje acetylen i siarkę elementarną. Tiofeny są klasycznie wytwarzane w reakcji 1,4-di ketonów , diestrów lub dikarboksylanów z odczynnikami siarczkującymi, takimi jak P 4 S 10, tak jak w syntezie tiofenu Paala-Knorra . Specjalistyczne tiofeny można syntetyzować w podobny sposób, stosując odczynnik Lawessona jako środek usiarczający lub w reakcji Gewalda , która polega na kondensacji dwóch estrów w obecności elementarnej siarki. Inną metodą jest cyklizacja Volharda – Erdmanna .
Tiofen jest produkowany na skromną skalę, wynoszącą około 2000 ton rocznie na całym świecie. Produkcja obejmuje reakcję w fazie gazowej źródła siarki, zwykle dwusiarczku węgla , i źródła C-4, zwykle butanolu . Odczynniki te kontaktuje się z katalizatorem tlenkowym w temperaturze 500–550 ° C.
Właściwości i struktura
W temperaturze pokojowej tiofen jest bezbarwną cieczą o łagodnie przyjemnym zapachu przypominającym benzen , z którym tiofen ma pewne podobieństwa. Wysoka reaktywność tiofenu w stosunku do sulfonowania jest podstawą oddzielenia tiofenu od benzenu, które są trudne do oddzielenia przez destylację ze względu na zbliżone temperatury wrzenia (różnica 4 ° C przy ciśnieniu otoczenia). Podobnie jak benzen, tiofen tworzy azeotrop z etanolem.
Cząsteczka jest płaska; kąt wiązania przy siarki wynosi około 93 °, kąt C – C – S wynosi około 109 °, a pozostałe dwa węgle mają kąt wiązania około 114 °. Wiązania C – C do atomów węgla sąsiadujących z siarką mają około 1,34 A , długość wiązania C – S około 1,70 A, a drugie wiązanie C – C około 1,41 A.
Reaktywność
Uważa się, że tiofen jest aromatyczny, chociaż obliczenia teoretyczne sugerują, że stopień aromatyczności jest mniejszy niż benzenu. „Pary elektronów” na siarki są znacznie zdelokalizowane w układzie elektronów pi . Ze względu na swoją aromatyczność tiofen nie wykazuje właściwości charakterystycznych dla konwencjonalnych siarczków . Na przykład atom siarki jest odporny na alkilowanie i utlenianie.
Utlenianie
Utlenianie może zachodzić zarówno przy siarki, dając S- tlenek tiofenu , jak i przy wiązaniu podwójnym 2,3, dając tiofen 2,3-epoksyd, po którym następuje rearanżacja przesunięcia NIH . Utlenianie tiofenu kwasem trifluoronadoctowym również wykazuje oba szlaki reakcji. Główny szlak tworzy S- tlenek jako półprodukt, który ulega późniejszej dimeryzacji typu Dielsa-Aldera i dalszemu utlenianiu, tworząc mieszaninę produktów sulfotlenkowych i sulfonowych o łącznej wydajności 83% (na podstawie dowodów NMR ):
W mniejszym szlaku reakcji epoksydacja Prilezhaeva skutkuje utworzeniem tiofeno-2,3-epoksydu, który szybko przestawia się w izomer tiofen-2-on. Pułapkujące eksperymenty wskazują, że droga ta nie jest reakcją uboczną Od? S -tlenku związku pośredniego, a znakowanie izotopowe z deuteru potwierdzają, że 1,2-wodorek przesunięcie wystąpi, a tym samym, że kationowy pośrednia jest zaangażowany. Jeśli mieszanina reakcyjna nie jest bezwodna , ten pomniejszy szlak reakcji jest tłumiony, ponieważ woda działa jako konkurencyjna zasada.
Utlenianie tiofenów może mieć znaczenie dla aktywacji metabolicznej różnych leków zawierających tiofen, takich jak kwas tienilowy i badany lek przeciwnowotworowy OSI-930.
Alkilacja
Chociaż atom siarki jest stosunkowo niereaktywny, flankujące centra węgla, pozycje 2 i 5, są bardzo podatne na atak elektrofilów . Halogeny dają początkowo pochodne 2-halo, a następnie 2,5-dihalotiofeny; perhalogenację można łatwo przeprowadzić, uzyskując C 4 X 4 S (X = Cl, Br, I). Bromian tiofenu jest 10 7 razy szybszy niż benzen.
Chlorometylacja i chloroetylacja zachodzą łatwo w pozycjach 2,5. Redukcja produktu chlorometylowego daje 2-metylotiofen. Hydroliza, a następnie odwodnienie ugrupowań chloroetylowych daje 2-winylotiofen.
Odsiarczanie niklem Raneya
Odsiarczanie tiofenu niklem Raneya daje butan . W połączeniu z łatwą 2,5-difunkcjonalizacją tiofenu, odsiarczanie zapewnia drogę do 1,4-dipodstawionych butanów.
Polimeryzacja
Polimer utworzony przez połączenie tiofenu w jego pozycjach 2,5 nazywany jest politiofenem . Polimeryzację prowadzi się przez utlenianie metodami elektrochemicznymi ( elektropolimeryzacja ) lub odczynnikami przenoszącymi elektrony. Pokazane jest wyidealizowane równanie:
- n C 4 H 4 S → (C 4 H 2 S) n + 2n H + + 2n e -
Sam politiofen ma słabe właściwości przetwórcze i dlatego jest mało zbadany. Bardziej przydatne są polimery pochodzące od tiofenów podstawionych w pozycjach 3, 3 i 4, takie jak EDOT (etylenodioksytiofen) . Po częściowym utlenieniu politiofeny stają się elektrycznie przewodzące, tzn. Uzyskują niektóre cechy charakterystyczne typowe dla metali.
Chemia koordynacyjna
Tiofen wykazuje niewielkie właściwości siarczkowe, ale służy jako pi-ligand tworzący kompleksy stolca fortepianu, takie jak Cr ( η 5 -C 4 H 4 S) (CO) 3 .
Pochodne tiofenu
- Niektóre tiofeny
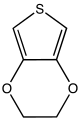
3,4-etylenodioksytiofen (EDOT) jest prekursorem komercyjnych wyświetlaczy antystatycznych i elektrochromowych .
Tienyl
Po deprotonowaniu tiofen przekształca się w grupę tienylową, C 4 H 3 S - . Chociaż anion sam w sobie nie istnieje, to pochodne litoorganiczne tak. Tak więc reakcja tiofenu z butylolitem daje 2-litiotiofen, zwany także 2-tienolitem. Odczynnik ten reaguje z elektrofilami, dając pochodne tienylu, takie jak tiol. Utlenianie tienylolitu daje 2,2'-dithienyl, (C 4 H 3 S) 2 . Do wytwarzania miedzianów mieszanych wyższego rzędu stosuje się tienylolit . Sprzęganie równoważników anionu tienylowego daje dithienyl , analog bifenylu.
Tiofeny zespolone z pierścieniem
Fuzja tiofenu z pierścieniem benzenowym daje benzotiofen . Fuzja z dwoma pierścieniami benzenowymi daje dibenzotiofen (DBT) lub naftiotiofen. Fuzja pary pierścieni tiofenowych daje izomery tienotiofenu .
Używa
Tiofeny są ważnymi związkami heterocyklicznymi, które są szeroko stosowane jako elementy budulcowe w wielu środkach agrochemicznych i farmaceutycznych. Pierścień benzenowy biologicznie czynnego związku można często zastąpić tiofenem bez utraty aktywności. Widać to na przykładach takich jak lornoksykam z NLPZ , tiofenowy analog piroksykamu i sufentanyl , tiofenowy analog fentanylu .
Bibliografia
Linki zewnętrzne
- Card International Bezpieczeństwa Chemicznego 1190
- Chisholm, Hugh, wyd. (1911). . Encyclopædia Britannica . 26 (wyd. 11). Cambridge University Press.