Dziedziczny obrzęk naczynioruchowy - Hereditary angioedema
| Dziedziczny obrzęk naczynioruchowy | |
|---|---|
| Inne nazwy | Dziedziczny obrzęk naczynioruchowy (HANE), rodzinny obrzęk naczynioruchowy |
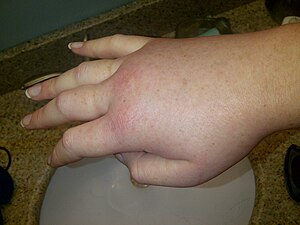 | |
| Opuchnięta prawa ręka podczas dziedzicznego napadu obrzęku naczynioruchowego. | |
| Specjalność | Hematologia |
| Objawy | Nawracające ataki silnego obrzęku |
| Zwykły początek | Dzieciństwo |
| Czas trwania | Ataki trwają kilka dni |
| Rodzaje | Typ I, II, III |
| Powoduje | Zaburzenie genetyczne ( autosomalne dominujące ) |
| Metoda diagnostyczna | Pomiar poziomów inhibitorów C4 i C1 . |
| Diagnostyka różnicowa | Niedrożność jelit , inne rodzaje obrzęku naczynioruchowego |
| Zapobieganie | Inhibitor C1 |
| Leczenie | Opieka podtrzymująca , leki |
| Lek | Inhibitor C1 , ekallantyd , ikatybant |
| Rokowanie | 25% ryzyko zgonu w przypadku zajęcia dróg oddechowych (bez leczenia) |
| Częstotliwość | ~1 na 50 000 |
Dziedziczny obrzęk naczynioruchowy ( HAE ) to zaburzenie, które powoduje nawracające ataki ciężkiego obrzęku . Obrzęk najczęściej dotyczy rąk, nóg, twarzy, przewodu pokarmowego i dróg oddechowych. W przypadku zajęcia przewodu pokarmowego mogą wystąpić bóle brzucha i wymioty . Obrzęk dróg oddechowych może spowodować ich niedrożność i trudności w oddychaniu. Bez leczenia zapobiegawczego ataki zwykle występują co dwa tygodnie i trwają kilka dni.
Istnieją trzy główne typy HAE. Typy I i II są spowodowane mutacją w genie SERPING1 , który tworzy białko inhibitorowe C1, podczas gdy typ III jest często spowodowany mutacją w genie F12 (czynnik XII). Rezultatem jest podwyższony poziom bradykininy , co sprzyja obrzękom. Choroba może być dziedziczona po rodzicach danej osoby w sposób autosomalny dominujący lub pojawiać się jako nowa mutacja. Wyzwalacze ataku mogą obejmować niewielki uraz lub stres, ale ataki często występują bez wyraźnego zdarzenia poprzedzającego. Rozpoznanie typu I i II opiera się na pomiarze poziomu inhibitorów C4 i C1.
Postępowanie z HAE obejmuje starania mające na celu zapobieganie napadom i leczenie napadów, jeśli wystąpią. Podczas ataku może być wymagana opieka wspomagająca, taka jak płyny dożylne i wspomaganie dróg oddechowych. Leki z grupy inhibitorów C1 można stosować zarówno w profilaktyce, jak i leczeniu, podczas gdy ekallantyd i ikatybant można stosować w leczeniu ostrych ataków.
HAE dotyka około 1 na 50 000 osób. Stan ten jest zwykle zauważany po raz pierwszy w dzieciństwie. Typ I i II w równym stopniu dotykały kobiety i mężczyzn, natomiast typ III częściej dotyka kobiety niż mężczyzn. W przypadku zajęcia dróg oddechowych bez leczenia ryzyko zgonu wynosi około 25%. Po leczeniu wyniki są na ogół dobre. Stan ten został po raz pierwszy opisany w 1888 roku przez kanadyjskiego lekarza Williama Oslera .
Symptomy i objawy
Osoby, u których zdiagnozowano dziedziczny obrzęk naczynioruchowy, mają nawracające obrzęki kończyn, narządów płciowych , twarzy , ust , krtani lub przewodu pokarmowego . Niektórzy pacjenci opisują uczucie pełności, ale nie ból lub swędzenie w dotkniętym obszarze, z wyjątkiem tych z obrzękiem brzucha, którzy często doświadczają ostrego bólu brzucha. Inni doświadczają intensywnego bólu, opisywanego jako promieniujący od kości na zewnątrz wraz z intensywnym swędzeniem tuż pod skórą i intensywnym ciepłem, niezależnie od docelowego obszaru.
Przypadki obrzęku wokół gardła lub krtani mogą powodować trudności w oddychaniu, jeśli obrzęk zatka drogi oddechowe. Wiadomo, że powoduje to dużą liczbę zgonów u osób dotkniętych tym zaburzeniem. Epizody atakujące przewód pokarmowy mogą powodować szereg powikłań, w tym odwodnienie spowodowane niezdolnością do powstrzymania czegokolwiek (co, w zależności od długości epizodu, może okazać się śmiertelne). Objawy obrzęku przewodu pokarmowego, w tym gwałtowne wymioty, silny ból brzucha, odwodnienie i intensywne wyczerpanie.
Niektóre osoby cierpiące na HAE doświadczają ataków „wędrujących”. Ataki te będą koncentrować się na kończynie. Na przykład: Jeśli ręka poszkodowanego puchnie, przejdzie przez normalny cykl obrzęku przed „przeniesieniem” do kończyny łączącej (w tym przypadku nadgarstka z przedramieniem) lub przesunie się do przeciwnej ręki. Osoby z tym objawem mogą uważać, że ich epizody trwają dłużej, a ich wyzwalacze mogą być trudniejsze do śledzenia.
Dziedzictwo
Ponieważ HAE jest chorobą autosomalną dominującą , nie ma różnic między płciami w przenoszeniu, a obie płcie mają jednakowe prawdopodobieństwo otrzymania zmutowanego genu od swoich rodziców. Na przykład ojciec (osoba A) ze zmutowanym genem HAE ma chorobę, podczas gdy jego żona (osoba B) z 2 niezmutowanymi kopiami genu inhibitora C1 nie ma choroby. Możliwość krzyżówki między nimi daje pokazane możliwości: dwoje z ich potomstwa będzie miało chorobę (HAE), a inne nie.
Chory ojciec, który ma HAE, ma mutację w jednym ze swoich genów (C1-INH). Każde z jego dzieci, niezależnie od płci, będzie miało 50% szans na odziedziczenie po nim zmutowanego genu C1-INH. HAE jest ogólnie określany jako stan „dominujący”, ponieważ do wywołania choroby wystarczy mutacja w jednym z dwóch genów C1-INH u nosiciela.
Częstość występowania HAE jest stosunkowo niska – od 1 na 10 000 do 1 na 50 000 osób. Większość osób z HAE nabywa mutację inhibitora C1 esterazy (C1-INH) od jednego z rodziców. Rodzic z HAE ma zwykle 50% prawdopodobieństwo przeniesienia tego stanu na jedno ze swoich dzieci obojga płci, jak pokazano na rysunku (Dziedziczenie HEA). Osoby bez wcześniejszej historii mogą nabyć HAE przez spontaniczne zmiany w plemniku lub komórce jajowej. W przeglądzie pacjentów, którzy nie mieli historii HAE w swojej rodzinie, ale którzy mają stosunkowo niski poziom zmutowanego C1-INH z utrzymującym się obrzękiem naczynioruchowym, 25% nowych pacjentów z HAE miało zmiany C1-INH, które nie wykazują objawów spadkowy.
Diagnoza
| C4 ( C ) | FB ( A ) | C3 | CH50 | Warunki |
|---|---|---|---|---|
| · | ↓ | ↓ | ↓ | PSG , C3 NeF AA |
| ↓ | · | ↓ | · | HAE , C4D |
| · | · | · | ↓ | TCPD |
| ↓ | · /↓ | ↓ | ↓ | SLE |
| ↑ | ↑ | ↑ | ↑ | zapalenie |
Rozpoznanie HAE jest często trudne ze względu na dużą zmienność ekspresji choroby. Przebieg choroby jest zróżnicowany i nieprzewidywalny, nawet u jednego pacjenta przez całe życie. Choroba ta może być podobna w swojej prezentacji do innych postaci obrzęku naczynioruchowego wynikającego z alergii lub innych schorzeń, ale różni się znacznie przyczynami i leczeniem. Kiedy HAE zostanie błędnie zdiagnozowana jako alergia, najczęściej leczy się ją sterydami i epinefryną, lekami, które zwykle są nieskuteczne w leczeniu epizodu HAE. Inne błędne diagnozy doprowadziły do niepotrzebnych operacji eksploracyjnych u pacjentów z obrzękiem brzucha, a inni pacjenci z HAE zgłaszają, że ich ból brzucha został błędnie zdiagnozowany jako psychosomatyczny.
HAE odpowiada tylko za niewielką część wszystkich przypadków obrzęku naczynioruchowego. Aby uniknąć potencjalnie śmiertelnych konsekwencji, takich jak niedrożność górnych dróg oddechowych i niepotrzebna operacja jamy brzusznej, nie można przecenić znaczenia prawidłowej diagnozy.
Należy wziąć pod uwagę HAE, jeśli u pacjenta występują:
- Nawracający obrzęk naczynioruchowy (bez pokrzywki)
- Nawracające epizody bólu brzucha i wymiotów
- Obrzęk krtani
- Pozytywny wywiad rodzinny dotyczący obrzęku naczynioruchowego
Badanie krwi, najlepiej wykonane podczas epizodu, może być wykorzystane do zdiagnozowania stanu. Miara: czynnik 4 dopełniacza w surowicy (C4), białko antygenowe inhibitora C1 (C1-INH), poziom czynnościowy inhibitora C1 (C1-INH), jeśli jest dostępny. Analiza poziomów inhibitora C1 dopełniacza może odgrywać rolę w diagnostyce. C4 i C2 to składniki uzupełniające się.
Rodzaje
Istnieją trzy rodzaje niedoboru inhibitora C1:
HAE typu I jest spowodowany głównie niedoborem białek krwi ( inhibitory esterazy C1 ), które normalnie hamują aktywację układu dopełniacza . Wynikająca z tego nadmierna stymulacja tego układu prowadzi do produkcji zapalnych anafilatoksyn , co wpływa na przepływ płynów ustrojowych między układem naczyniowym a tkankami organizmu. Ten niedobór odpowiada za około 80-85% przypadków.
HAE typu II jest rzadziej spotykaną postacią tego zaburzenia i stanowi 15–20% przypadków. W tym typie wytwarzane są nietypowe białka inhibitorowe C1, które są mniej zdolne do hamowania aktywacji układu dopełniacza. Podobnie jak HAE typu I, powoduje to nadmierną stymulację tego układu.
HAE typu III jest rzadki i dopiero niedawno został udokumentowany. W przeciwieństwie do typów I i II, ta forma nie wydaje się być związana z niedoborem inhibitora C1. Ten typ dotyka głównie kobiety i wydaje się, że ma na niego wpływ kontakt z estrogenami, a także hormonalna terapia zastępcza (np. doustne środki antykoncepcyjne). Jej patogenezie przypisuje się zwiększoną aktywność enzymu kininogenazy, co prowadzi do wzrostu poziomu bradykininy . Inni pacjenci z HAE typu III mają zmiany w genie F12, który koduje białko biorące udział w krzepnięciu krwi . Niektórzy pacjenci z HAE typu III mają mutację w genie F12, który wytwarza białko biorące udział w krzepnięciu krwi. Ze względu na wyniki badań genetycznych u 4 dotkniętych rodzin niemieckich uważa się, że przyczyną tego typu schorzenia jest gen chorobotwórczy w chromosomie 5q.35.2-q35.3.
Zapobieganie
Leczenie inhibitorami ACE jest przeciwwskazane w tym stanie, ponieważ leki te mogą prowadzić do akumulacji bradykininy, co może przyspieszyć epizody choroby.
Długoterminowy
Osoby, u których epizody występują co najmniej raz w miesiącu lub u których występuje duże ryzyko wystąpienia obrzęku krtani, wymagają długoterminowej profilaktyki. Istnieje kilka badań klinicznych III fazy dotyczących profilaktyki i terapii HAE. Doprowadziło to do licencjonowania pdC1INH w wielu częściach świata; antagoniści receptora bradykininy ( ikatybant ) w Europie; inhibitory kalikreiny ( ekallantyd i lanadelumab ) w Stanach Zjednoczonych; oraz rekombinowaną terapię zastępczą C1-INH (rhC1INH; konestat alfa) w Europie. Wykazano, że kwas traneksamowy jest stosunkowo nieskuteczną terapią. Danazol profilaktyka pozostaje opcją, ale środki terapeutyczne są obecnie wykorzystywane w profilaktyce bardziej z powodu zdarzeń niepożądanych Danazol jest. Dla osób wymagających długotrwałej profilaktyki terapia domowa, która umożliwia samodzielne podawanie produktu, jest uważana za integralną część zapewnienia pacjentom normalnej jakości życia.
W 2018 roku, US Food and Drug Administration zatwierdzony lanadelumab , iniekcji monoklonalnego przeciwciała , w celu zapobiegania atakom HAE typów I i II u pacjentów w wieku powyżej 12 Lanadelumab hamuje enzym plazma kalikreina , który uwalnia kininy bradykininy i kallidin z ich kininogen prekursorów i jest wytwarzany w nadmiarze u osób z HAE typu I i II.
Berotralstat został zatwierdzony w Stanach Zjednoczonych w grudniu 2020 r. w celu zapobiegania atakom dziedzicznego obrzęku naczynioruchowego u osób powyżej dwunastego roku życia.
Krótkoterminowe
Profilaktykę krótkoterminową zwykle stosuje się przed zabiegiem chirurgicznym lub leczeniem stomatologicznym. W Niemczech do tego celu stosuje się koncentrat C1-INH, który podaje się 1-1,5 godziny przed zabiegiem. W krajach, w których koncentrat inhibitora C1 nie jest dostępny lub jest dostępny tylko w nagłych wypadkach (obrzęk krtani), leczenie wysokimi dawkami androgenów stosuje się przez 5–7 dni.
Kierownictwo
Celem leczenia doraźnego jest jak najszybsze zatrzymanie progresji obrzęku , co może uratować życie, zwłaszcza jeśli obrzęk znajduje się w krtani . W Niemczech najbardziej doraźne leczenie składa się z koncentratu inhibitora C1 z krwi dawcy, który należy podawać dożylnie; jednak w większości krajów europejskich koncentrat inhibitora C1 jest dostępny tylko dla pacjentów uczestniczących w specjalnych programach. W sytuacjach nagłych, gdy koncentrat inhibitora C1 nie jest dostępny, można alternatywnie użyć świeżo mrożonego osocza (FFP), ponieważ zawiera ono również inhibitor C1.
Inne sposoby leczenia mogą stymulować syntezę inhibitora C1 lub zmniejszać zużycie inhibitora C1. Oczyszczony inhibitor C1, pochodzący z ludzkiej krwi, jest stosowany w Europie od 1979 roku. Kilka terapii inhibitorami C1 jest obecnie dostępnych w amerykańskiej Agencji ds. Żywności i Leków, a dwa produkty z inhibitorami C1 są obecnie dostępne w Kanadzie. Pasteryzowany Berinert P (CSL Behring) został zatwierdzony przez FDA w 2009 roku do stosowania w ostrych atakach. Cinryze (ViroPharma), który jest nanofiltrowany, został zatwierdzony przez FDA w 2008 roku do profilaktyki. Ruconest (Pharming) to rekombinowany inhibitor C1 zatwierdzony w USA i Europie, który nie niesie ryzyka przeniesienia chorób zakaźnych z powodu patogenów krwiopochodnych.
Lek ekallantyd hamuje kalikreinę osocza i został zatwierdzony przez FDA (ale nie w Europie) do stosowania w ostrych atakach w 2009 roku. Ikatybant hamuje receptor bradykininy B2 i został dopuszczony w Europie i USA. W HAE może być konieczne unikanie w przyszłości określonych bodźców, które wcześniej prowadziły do ataków. Nie reaguje na leki przeciwhistaminowe , kortykosteroidy lub epinefrynę .
Rokowanie
Około 25% osób dotkniętych chorobą umiera w ciągu pierwszych dwóch dekad życia, głównie z powodu braku leczenia.
Epidemiologia
Dane dotyczące epidemiologii obrzęku naczynioruchowego są ograniczone. Częstość występowania HAE to jedna na 10 000-50 000 osób w Stanach Zjednoczonych i Kanadzie. Śmiertelność szacuje się na 15–33%, wynikającą głównie z obrzęku krtani i uduszenia. HAE prowadzi do 15 000-30 000 wizyt na oddziałach ratunkowych rocznie.
Społeczeństwo i kultura
W wielu krajach na całym świecie istnieją krajowe stowarzyszenia pacjentów z HAE i ich rodzin. Te krajowe stowarzyszenia są członkami globalnej organizacji HAEi – Międzynarodowej Organizacji Pacjentów ds. Niedoborów inhibitorów C1. HAEi zajmuje się podnoszeniem świadomości niedoborów inhibitorów C1 na całym świecie. Jest to międzynarodowa sieć non-profit, ustanowiona w celu promowania współpracy, koordynacji i wymiany informacji między specjalistami HAE i krajowymi stowarzyszeniami pacjentów z HAE w celu ułatwienia dostępności skutecznej diagnozy i leczenia niedoborów inhibitorów C1 na całym świecie.
Assistance Fund Inc. jest amerykańską organizacją non-profit, która oferuje współpłatną pomoc w leczeniu HAE i jest otwarta dla wszystkich obywateli amerykańskich lub imigrantów z ziemią, którzy posiadają ubezpieczenie.
Lisa Sanders opisała kiedyś przypadek w swojej kolumnie w czasach nowojorskich o tajemniczym przypadku dziedzicznego obrzęku naczynioruchowego spowodowanego tabletkami antykoncepcyjnymi
Badania
Obecnie trwa rozwój kliniczny kilku nowych substancji czynnych, które na różne sposoby interweniują w proces chorobowy.
Pharming Group NV poinformowała 24 czerwca 2010 r., że Europejska Agencja Leków przyjęła pozytywną opinię dotyczącą konestatu alfa (nazwa handlowa Ruconest), inhibitora C1 stosowanego w leczeniu ostrych napadów obrzęku naczynioruchowego.
Ekallantyd , peptydowy inhibitor kalikreiny , otrzymał status sierocego HAE i wykazał pozytywne wyniki w badaniach III fazy.
Ikatybant (sprzedawany jako Firazyr) jest selektywnym antagonistą receptora bradykininy , który został zarejestrowany w Europie i zatwierdzony w USA przez FDA w sierpniu 2011 roku. Po początkowych, granicznych wynikach lek ten okazał się skuteczny w badaniach III fazy. Cinryze została zatwierdzona przez FDA w październiku 2008 roku.
Bibliografia
Dalsza lektura
- Busse PJ, Christiansen SC (marzec 2020). „Dziedziczny obrzęk naczynioruchowy”. N. Engl. J. Med . 382 (12): 1136–48. doi : 10.1056/NEJMra1808012 . PMID 32187470 .
Zewnętrzne linki
| Klasyfikacja | |
|---|---|
| Zasoby zewnętrzne |
