Receptor 5-HT 2C -5-HT2C receptor
5-HT 2C receptora jest podtypem receptora 5-HT , które wiąże się z endogennego neuroprzekaźnika serotoniny (5-hydroksytryptaminy, 5-HT). Jest sprzężony z białkiem G receptora (GPCR), który jest połączony z G Q / G 11 i pośredniczy pobudzenia neurotransmisji . HTR2C oznacza ludzki gen kodujący receptor , który u ludzi znajduje się na chromosomie X. Ponieważ mężczyźni mają jedną kopię genu, au kobiet jedna z dwóch kopii genu jest stłumiona, polimorfizmy w tym receptorze mogą wpływać na obie płcie w różnym stopniu.
Struktura
Na powierzchni komórki receptor istnieje jako homodimer . Struktura krystaliczna znana jest od 2018 roku.
Dystrybucja
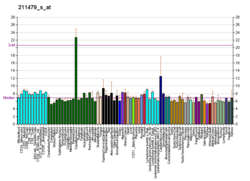
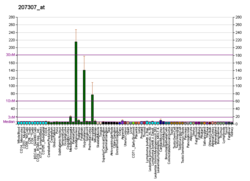
Receptory 5- HT2C zlokalizowane są głównie w splocie naczyniówkowym, au szczurów występują w dużych stężeniach również w wielu innych obszarach mózgu, w tym w częściach hipokampu , przednim jądrze węchowym , istocie czarnej , kilku jądrach pnia mózgu , ciele migdałowatym , jądrze podwzgórzowym i habenula boczna . Receptory 5-HT 2C znajdują się również na komórkach nabłonkowych wyścielających komory .
Funkcjonować
Receptor 5- HT2C jest jednym z wielu miejsc wiązania serotoniny . Aktywacja tego receptora przez serotoninę hamuje uwalnianie dopaminy i noradrenaliny w niektórych obszarach mózgu.
Twierdzi się, że receptory 5- HT2C znacząco regulują nastrój, lęk, karmienie i zachowania reprodukcyjne. Receptory 5- HT2C regulują między innymi uwalnianie dopaminy w prążkowiu , korze przedczołowej , jądrze półleżącym , hipokampie , podwzgórzu i ciele migdałowatym .
Badania wskazują, że niektóre ofiary samobójstw mają nienormalnie wysoką liczbę receptorów 5-HT 2C w korze przedczołowej. Agomelatyna , będąca antagonistą 5-HT 2C i 5-HT 2B oraz agonistą MT 1 i MT 2 , jest skutecznym antydepresantem . Nazywany jest lekiem odhamowującym norepinefryno-dopaminę, ponieważ antagonizm receptorów 5-HT 2C przez agomelatynę powoduje wzrost aktywności dopaminy i norepinefryny w korze czołowej. Odwrotnie, wiele SSRI (ale nie fluoksetyna , która jest antagonistą 5-HT 2C ) pośrednio stymuluje aktywność 5-HT 2C poprzez zwiększenie poziomu serotoniny w synapsie, chociaż opóźnione podniesienie nastroju, które jest zwykle typowe dla SSRI, jest zwykle połączone z obniżeniem receptorów 5- HT2C . Wiele atypowych leków przeciwpsychotycznych blokuje receptory 5-HT 2C , ale ich kliniczne zastosowanie jest ograniczone przez liczne niepożądane działania na różne neuroprzekaźniki i receptory . Fluoksetyna działa jako bezpośredni antagonista 5- HT2C , oprócz hamowania wychwytu zwrotnego serotoniny , jednakże kliniczne znaczenie tego działania jest zmienne. Kilka tetracyklicznych leków przeciwdepresyjnych , w tym mirtazapina , jest silnymi antagonistami 5- HT2C ; działanie to może przyczynić się do ich skuteczności.
Nadaktywność receptorów 5-HT 2C może przyczyniać się do wystąpienia objawów depresyjnych i lękowych w pewnej populacji pacjentów. Aktywacja 5-HT 2C przez serotoninę jest odpowiedzialna za wiele negatywnych skutków ubocznych leków SSRI i SNRI , takich jak sertralina , paroksetyna , wenlafaksyna i inne. Część początkowego niepokoju wywołanego przez SSRI jest spowodowana nadmierną sygnalizacją w 5- HT2C . W ciągu 1-2 tygodni, receptor zaczyna obniżają wraz z podregulacją 5-HT 2A , 5-HT1 A i innych receptorów serotoniny. Ta regulacja w dół jest zbieżna z początkiem klinicznych korzyści SSRI. Receptory 5- HT2C wykazują konstytutywną aktywność in vivo i mogą zachowywać zdolność wpływania na neuroprzekaźnictwo przy braku zajęcia ligandu. Zatem receptory 5- HT2C nie wymagają wiązania przez ligand (serotoninę), aby wykazywać wpływ na neuroprzekaźnictwo. Odwrotni agoniści mogą być potrzebni do pełnego wygaszenia konstytutywnej aktywności 5- HT2C i mogą okazać się użyteczni w leczeniu stanów, w których pośredniczy 5- HT2C przy braku typowej aktywności serotoniny. Oprócz dowodów na rolę stymulacji receptora 5-HT 2C w objawach depresji, istnieją również dowody na to, że aktywacja receptorów 5-HT 2C może mieć korzystny wpływ na pewne aspekty depresji, jedna grupa badaczy stwierdziła, że bezpośrednia stymulacja 5 Receptory -HT 2C z agonistą 5-HT 2C zmniejszały deficyty poznawcze u myszy z mutacją utraty funkcji TPH2 .
Receptory 5- HT2C pośredniczą w uwalnianiu i zwiększeniu zewnątrzkomórkowej dopaminy w odpowiedzi na wiele leków, w tym kofeinę , nikotynę , amfetaminę , morfinę , kokainę i inne. Antagonizm 5-HT 2C zwiększa uwalnianie dopaminy w odpowiedzi na leki wzmacniające i wiele bodźców dopaminergicznych. Karmienie, interakcje społeczne i aktywność seksualna - wszystkie uwalniają dopaminę podlegającą inhibicji 5- HT2C . Zwiększona ekspresja 5- HT2C zmniejsza uwalnianie dopaminy zarówno w obecności, jak i przy braku bodźców.
Warunki, które zwiększają poziom cytokin w ludzkim ciele, mogą potencjalnie zwiększać ekspresję genu 5-HT 2C w mózgu. Może to prawdopodobnie obejmować związek między infekcjami wirusowymi a związaną z nimi depresją. Wykazano, że terapia cytokinami zwiększa ekspresję genu 5-HT 2C , powodując zwiększoną aktywność receptorów 5-HT 2C w mózgu.
Endokrynologia
Serotonina jest zaangażowany w podstawowej i regulacji naprężenia wywołane podwzgórza i przysadki hormony takie jak prolaktyna , hormon adrenokortykotropowy ( ACTH ), wazopresyny i oksytocyny , głównie poprzez działania podtypów receptora 5-HT 2A, 5-HT 2C . Dlatego receptor 5- HT2C jest istotnym modulatorem osi podwzgórze-przysadka-nadnercza ( oś HPA ). Oś HPA jest głównym kontrolerem ostrych współczulnych reakcji stresowych związanych z reakcją walki lub ucieczki . Przedłużona aktywacja i zaburzenia osi HPA przyczyniają się do wystąpienia objawów depresyjnych i lękowych obserwowanych w wielu stanach psychopatologicznych.
Stymulacja receptorów 5- HT2C prowadzi do wzrostu mRNA hormonu uwalniającego kortykotropinę ( CRH ) i wazopresyny w jądrze przykomorowym oraz proopiomelanokortyny w przednim płacie przysadki. U szczurów stres powstrzymujący (który może powodować objawy depresji, jeśli jest przewlekły) indukuje wydzielanie prolaktyny, ACTH, wazopresyny i oksytocyny, w którym częściowo pośredniczy receptor 5- HT2C . Odpowiedzi w takich stanach jak odwodnienie lub krwotok powodują uwalnianie oksytocyny poprzez odpowiedź serotonergiczną, w której częściowo pośredniczy 5- HT2C . Ponadto, obwodowe uwalnianie wazopresyny obejmuje odpowiedź serotonergiczną, w której częściowo pośredniczy 5- HT2C .
Ekspresja receptora 5- HT2C w OUN jest modulowana przez żeńskie hormony płciowe estradiol i progesteron . Kombinacja hormonów zmniejsza stężenie receptorów w hipokampie brzusznym u szczurów i może w ten sposób wpływać na nastrój.
Genetyka
Zidentyfikowano wiele ludzkich polimorfizmów wpływających na ekspresję 5- HT2C . Sugerowane są istotne korelacje, szczególnie w odniesieniu do zaburzeń psychicznych, takich jak depresja, OCD i stany lękowe. Polimorfizmy korelują również z podatnością na szereg schorzeń, w tym zaburzenia używania substancji i otyłość . Istnieją przesłanki, że alternatywny splicing receptora 5- HT2C jest regulowany przez snoRNA o nazwie SNORD115 , którego delecja jest związana z zespołem Pradera-Williego . Ponieważ ludzki gen znajduje się w chromosomie X, mężczyźni mają tylko jedną kopię genu, podczas gdy kobiety mają dwie, co oznacza, że mutacje w genie wpływają na fenotyp mężczyzny, nawet jeśli allel miałby charakter recesywny. Ponieważ kobiety mają dwie kopie genu, ale tylko jeden allel jest wyrażany w każdej komórce, stanowią one mozaikę polimorfizmów, co oznacza, że jeden wariant genetyczny może dominować w jednej tkance, a inny wariant będzie dominować w innej tkance (jak w przypadku wszystkie inne odmiany genetyczne sprzężone z chromosomem x).
Ligandy
Pierwsze modulatory allosteryczne zostały opracowane w 2018 roku.
Agoniści
- A-372,159
- AL-38022A
- CP-809,101
- CPD-1
- Fenfluramina
- Lisuride
- Lorcaserin
- Mesulergina
- MK-212
- Naftyloizopropyloamina
- Norfenfluramina
- Organizacja 12 962
- ORG-37,684
- Oksaflozan
- PF-04479745
- PNU-22394
- PNU-181731
-
Psychodeliki
- Lizergamidy ( LSD itp.)
- Fenetylaminy ( 2C-B , DOI , DOM , meskalina itp.)
- Piperazyny ( mCPP , TFMPP , itp.)
- Tryptaminy ( 5-MeO-DMT , Bufotenina , DMT , Psilocin , etc.)
- Ro60-0175
- Wabikazerin
- DROGA-629
- DROGA-161,503
- DROGA-163.909
- YM-348
- CP-132484 również agonista 5HT2a.
Częściowi agoniści
Antagoniści
- Agomelatyna
- CEPC
- Eltoprazyna
- Etoperidon
- Flibanseryna
- Fluoksetyna
- FR-260,010
- Tedatioksetyna
- Metysergid
- Mirtazapina
- Nefazodon
- Norfluoksetyna
- O-desmetylotramadol
- Prometazyna
- RS-102,221
- SB-200.646
- SB-221,284
- SB-228,357
- SB-242,084
- SDZ SER-082
- Tramadol
- Trazodon
Odwrotni agoniści
-
Antydepresanty
- Trójpierścieniowe ( amitryptylina , klomipramina , imipramina , Nortryptylina , doksepina , itd.)
- Tetracykliczne ( Mirtazapina , mianseryna , amoksapinę , etc.)
- Leki przeciwhistaminowe ( Cyproheptadyna , Hydroksyzyna , Latrepirdyna , itp.)
-
Leki przeciwpsychotyczne
- Typicals ( chlorpromazyna , flufenazyna , loksapina , tiorydazyna , etc.)
- Nietypowe ( klozapina , olanzapina , kwetiapina , risperidon , zyprazydon itp.)
- Cynanseryna
- Deramcyklan
- ketanseryna
- LY-53,857
- Metergolina
- Metiotepina
- Pizotifen
- Ritanseryna
- S-32212
- SB-206,553
- SB-228,357
- SB-243,213
- SB-242,084
Interakcje
Wykazano, że receptor 5- HT2C oddziałuje z MPDZ .
Edycja RNA
Pre-mRNA 5HT2CR może być przedmiotem edycji RNA . Jest to jedyny receptor serotoniny, a także jedyny członek dużej rodziny 7 receptorów transbłonowych (7TMR), o których wiadomo, że jest edytowany. Różne poziomy edycji skutkują różnorodnymi efektami na funkcję receptora.
Rodzaj
Rodzaj edycji RNA, który występuje w pre-mRNA 5HT2CR to edycja z adenozyny na inozynę (od A do I).
Edycja RNA A do I jest katalizowana przez rodzinę deaminaz adenozynowych działających na RNA (ADAR), które specyficznie rozpoznają adenozyny w dwuniciowych regionach pre-mRNA i deaminują je do inozyny . Inozyny są rozpoznawane jako guanozyna przez maszynerię translacyjną komórek. Istnieją trzej członkowie rodziny ADAR, ADAR 1-3, przy czym ADAR1 i ADAR2 są jedynymi aktywnymi enzymatycznie członkami. Uważa się, że ADAR3 odgrywa rolę regulacyjną w mózgu. ADAR1 i ADAR2 są szeroko wyrażane w tkankach, podczas gdy ADAR3 jest ograniczone do mózgu. Dwuniciowe regiony RNA są tworzone przez parowanie zasad między resztami w bliskim regionie miejsca edycji z resztami zwykle w sąsiednim intronie, ale mogą być sekwencją egzonową. Region, który paruje zasad z regionem edycyjnym, jest znany jako edycyjna sekwencja komplementarna (ECS).
ADAR wiążą się bezpośrednio z substratem dsRNA poprzez swoje domeny wiążące dwuniciowe RNA. Jeśli miejsce edycji występuje w sekwencji kodującej, może to spowodować zmianę kodonu. Może to prowadzić do translacji izoformy białka ze względu na zmianę jego pierwotnej struktury białkowej. Dlatego edycja może również zmienić funkcję białka. Edycja A do I zachodzi w niekodujących sekwencjach RNA, takich jak introny , regiony niepodlegające translacji (UTR), LINIE , SINE (zwłaszcza powtórzenia Alu). Uważa się, że funkcja edycji A do I w tych regionach obejmuje tworzenie miejsc splicingu i zachowanie m.in. RNA w jądrze.
Lokalizacja
Edycja zachodzi w 5 różnych blisko położonych miejscach w eksonie 5, co odpowiada drugiej pętli wewnątrzkomórkowej końcowego białka. Miejsca te są znane jako A, B, C′ (wcześniej nazywane E), C i D i przewiduje się, że występują w pozycjach aminokwasów 156, 158 i 160. Kilka zmian kodonów może wystąpić z powodu edycji A-do-I w te witryny. Mogą wystąpić 32 różne warianty mRNA prowadzące do 24 różnych izoform białek.
- Izoleucyna do Waliny (I/V) w pozycji aminokwasu 157,161.
- Izoleucyna do metioniny (I/M) w pozycji aminokwasu 157
- Asparaginian do seryny (N/S) o 159
- Asparaginian do asparaginy (N/D) w 159
- Asparagina do glicyny (N/G) w 159.
Te zmiany kodonów, które mogą wystąpić z powodu edycji A do I w tych miejscach, mogą prowadzić do maksymalnie 32 różnych wariantów mRNA prowadzących do 24 różnych izoform białek. Liczba izoform białek jest mniejsza niż 32, ponieważ niektóre aminokwasy są kodowane przez więcej niż jeden kodon. Inne miejsce edycji, miejsce F, zostało również zlokalizowane w sekwencji komplementarnej do eksonu (ECS) intronu 5. ECS wymagany do utworzenia dwuniciowej struktury RNA znajduje się w intronie 5.
Ochrona
Edycja RNA tego receptora zachodzi w 4 miejscach u szczura. Edycja odbywa się również za pomocą myszy. Wstępna demonstracja edycji RNA u szczura. Dominującą izoformą w mózgu szczura jest VNV, który różni się od najpowszechniejszego typu występującego u ludzi. Wiadomo, że edytująca sekwencja komplementarna jest zachowana w całej Mammalia.
Rozporządzenie
5-HT 2c receptora serotoniny jest jedynym receptorem edytowany pomimo swoich bliskich podobieństwa sekwencji do innych członków rodziny. 5HT2CR jest inny ze względu na posiadanie niedoskonałych odwróconych powtórzeń na końcu eksonu 5 i na początku intronu 5, co umożliwia tworzenie dupleksu RNA wytwarzającego dsRNA wymagane przez ADAR do edycji. Wykazano, że zakłócenie tego odwróconego powtórzenia powoduje zaprzestanie wszelkiej edycji. Różne izoformy mRNA 5HT2CR ulegają różnej ekspresji w mózgu, jednak nie wszystkie z 24 zostały wykryte być może ze względu na ekspresję specyficzną dla tkanki lub edycję z niską częstotliwością określonego typu. Te izoformy, które nie są wyrażane w ogóle lub z bardzo niską częstotliwością, są łączone poprzez edycję tylko w witrynie C' i/lub witrynie B, ale nie w witrynie A. Kilka przykładów różnic w częstotliwości edycji i edycji witryny w różnych częściach ludzki mózg 5HT2CR ma niską częstotliwość edycji w móżdżku i prawie cała edycja odbywa się w miejscu D, podczas gdy w hipokampie częstotliwość edycji jest wyższa, gdzie miejsce A jest głównym miejscem edycji. Miejsce C' znajduje się tylko w wersji edytowanej we wzgórzu. Najczęstszą izoformą w ludzkim mózgu jest izoforma VSV.
Nokaut myszy i inne badania zostały wykorzystane do określenia, który enzym ADAR jest zaangażowany w edycję. Wykazano, że edycja w miejscach A i B jest spowodowana edycją ADAR1. Również ponieważ ekspresja ADAR1 jest zwiększona w odpowiedzi na obecność interferonu a, zaobserwowano również, że edycja w miejscach A i B również została zwiększona z tego powodu. Miejsca C' i D wymagają ADAR2, a edycja jest zmniejszona przez obecność ADAR1 z edycją miejsca C' obserwowaną tylko u myszy z podwójnym knock-outem ADAR1. Wykazano, że miejsce C jest głównie edytowane przez ADAR2, ale w obecności podwyższonej ekspresji ADAR1, nastąpił wzrost edycji tego miejsca, a obecność enzymów może również skutkować ograniczoną edycją u myszy z nokautem ADAR2. Pokazuje to, że musi istnieć jakaś interakcja między dwoma enzymami edycyjnymi A do I. Również takie interakcje i specyficzna tkankowo ekspresja interakcji ADAR mogą wyjaśniać różnorodność wzorców edycji w różnych obszarach mózgu.
Konsekwencje
Po drugie, wzór edycji kontroluje ilość mRNA 5-HT2CR, która prowadzi do ekspresji białka pełnej długości poprzez modulację wyboru miejsca alternatywnego splicingu 76,77. Spośród trzech alternatywnych miejsc donorowych splicingu (GU1 do GU3; Fig. 4C), GU2 jest jedynym miejscem, które tworzy dojrzałe mRNA do produkcji funkcjonalnego białka 5-HT2CR o pełnej długości. Nieedytowane pre-mRNA mają tendencję do składania w miejscu GU1, co skutkuje skróconym, niefunkcjonalnym białkiem po translacji 76,77. Jednak większość pre-mRNA edytowanych w więcej niż jednej pozycji jest składana w GU2 77. Tak więc, gdy edycja jest nieefektywna, zwiększony splicing w GU1 może działać jako mechanizm kontrolny w celu zmniejszenia biosyntezy 5-HT2CR-INI, a tym samym ograniczenia odpowiedzi serotoniny . Po trzecie, edycja RNA kontroluje ostateczną fizjologiczną produkcję konstytutywnie aktywnych receptorów, wpływając na ekspresję 5-HT2CR na powierzchni komórki. 5-HT2CR-VGV, który wykazuje najniższy poziom konstytutywnej aktywności, jest w pełni wyrażany na powierzchni komórki w warunkach podstawowych i jest szybko internalizowany w obecności agonisty 78. W przeciwieństwie do tego 5-HT2CR-INI jest konstytutywnie internalizowany i gromadzi się w endosomach 78.
Struktura
Jak wspomniano, edycja powoduje kilka zmian kodonów. Miejsca edycji znajdują się w drugiej domenie wewnątrzkomórkowej białka, która jest również domeną sprzęgającą receptory białka G. Dlatego edycja tych miejsc może wpływać na powinowactwo receptora do wiązania białka G.
Funkcjonować
Edycja skutkuje zmniejszonym powinowactwem do określonych białek G, co z kolei wpływa na sygnalizację wewnętrzną za pośrednictwem wtórnych przekaźników (system sygnalizacji fosfolipazy C). W pełni edytowana izoforma VGV znacznie zmniejsza siłę działania 5-HT, sprzęganie białka G i wiązanie agonisty w porównaniu z niezmodyfikowaną izoformą białka INI. 72-76. Większość dowodów na wpływ edycji na funkcję pochodzi z dalszych pomiarów aktywności receptora, wiązania radioligandów i badań funkcjonalnych. Efekty hamujące są powiązane z zakresem edycji. Te izoformy o wyższym poziomie edycji wymagają wyższych poziomów serotoniny do aktywacji szlaku fosfolipazy c. Nieedytowana forma INI ma większą tendencję do izomeryzacji do formy aktywnej, która może łatwiej wchodzić w interakcje z białkami G. Wskazuje to, że edycja RNA może być tutaj mechanizmem regulacji pobudliwości neuronalnej poprzez stabilizację sygnalizacji receptora.
Uważa się również, że edycja działa na ekspresję podtypu receptora na powierzchni komórki. W pełni edytowany VGV, który ma najniższy poziom konstytutywnej aktywności, ulega pełnej ekspresji na powierzchni komórki, podczas gdy nieedytowany INI ulega internalizacji i akumuluje w endosomie.
Uważa się również, że edycja ma wpływ na splicing. Istnieją trzy różne izoformy złożonego receptora. Edycja reguluje ilość mRNA 5HT2CR, co prowadzi do translacji selekcji białka pełnej długości z alternatywnych miejsc składania. t76,77. Te miejsca splicingu są określane jako Gu1, Gu2, GU3. Tylko splicing miejsca GU2 skutkuje translacją receptora pełnej długości, podczas gdy wiadomo, że edycja w GU1 powoduje translację skróconego białka. Uważa się, że jest to mechanizm regulacyjny, który zmniejsza ilość nieedytowanej izoformy INI w celu ograniczenia odpowiedzi serotoniny, gdy edycja jest nieefektywna. Większość edytowanych pre-mRNA jest poddawana splicingowi w miejscu GU2.
Rozregulowanie
Rodzina receptorów serotoninowych jest często powiązana z patologią kilku ludzkich stanów psychicznych, takich jak schizofrenia, lęk, choroba afektywna dwubiegunowa i poważna depresja. Przeprowadzono kilka eksperymentalnych badań nad skutkami alternatywnych wzorców edycji 5HT2CR i tych warunków z dużą zmiennością wyników, szczególnie tych odnoszących się do schizofrenii. Niektóre badania wykazały wzrost edycji RNA w miejscu A u ofiar samobójstw w depresji. Zaobserwowano zwiększoną edycję strony E u osób cierpiących na poważną depresję. W modelach szczurzych ten wzrost jest również obserwowany i można go odwrócić za pomocą fluoksetyny, z pewną sugestią, że edycja miejsca E może być powiązana z poważną depresją.
Zobacz też
Bibliografia
Zewnętrzne linki
- Lokalizacja genomu ludzkiego HTR2C i strona szczegółów genu HTR2C w przeglądarce genomu UCSC .
- Przegląd wszystkich informacji strukturalnych dostępnych w PDB dla UniProt : P28335 (5-hydroksytryptaminowy receptor 2C) w PDBe-KB .
Dalsza lektura
- Niswender CM, Sanders-Bush E, Emeson RB (grudzień 1998). „Identyfikacja i charakterystyka zdarzeń edycji RNA w obrębie receptora 5-HT2C”. Roczniki Nowojorskiej Akademii Nauk . 861 (1): 38–48. Kod Bib : 1998NYASA.861...38N . doi : 10.1111/j.1749-6632.1998.tb10171.x . PMID 9928237 . S2CID 25127011 .
- Hoyer D, Hannon JP, Martin GR (kwiecień 2002). „Molekularna, farmakologiczna i funkcjonalna różnorodność receptorów 5-HT”. Farmakologia Biochemia i zachowanie . 71 (4): 533–54. doi : 10.1016/S0091-3057(01)00746-8 . PMID 11888546 . S2CID 25543069 .
- Raymond JR, Mukhin YV, Gelasco A, Turner J, Collinsworth G, Gettys TW, Grewal JS, Garnovskaya MN (2002). „Wiele mechanizmów transdukcji sygnału receptora serotoniny”. Farmakologia i terapia . 92 (2–3): 179–212. doi : 10.1016/S0163-7258(01)00169-3 . PMID 11916537 .
- Van Oekelen D, Luyten WH, Leysen JE (kwiecień 2003). „Receptory 5-HT2A i 5-HT2C oraz ich nietypowe właściwości regulacyjne”. Nauki o życiu . 72 (22): 2429–49. doi : 10.1016/S0024-3205(03)00141-3 . PMID 12650852 .
- Reynolds GP, Templeman LA, Zhang ZJ (lipiec 2005). „Rola polimorfizmów receptora 5-HT2C w farmakogenetyce leczenia lekami przeciwpsychotycznymi”. Postęp w Neuro-Psychofarmakologii i Psychiatrii Biologicznej . 29 (6): 1021–8. doi : 10.1016/j.pnpbp.2005.03.019 . PMID 15953671 . S2CID 30964513 .
- Millana MJ (2006). „Receptory serotoniny 5-HT2C jako cel w leczeniu stanów depresyjnych i lękowych: skupienie się na nowych strategiach terapeutycznych”. Terapia . 60 (5): 441–60. doi : 10.2515/terapia: 2005065 . PMID 16433010 .
- Milatovich A, Hsieh CL, Bonaminio G, Tecott L, Julius D, Francke U (grudzień 1992). „Gen receptora serotoniny 1c przypisany do chromosomu X u człowieka (prążek q24) i myszy (prążki D-F4)”. Genetyka molekularna człowieka . 1 (9): 681–4. doi : 10,1093/hmg/1,9681 . PMID 1302605 .
- Saltzman AG, Morse B, Whitman MM, Ivanshchenko Y, Jaye M, Felder S (grudzień 1991). „Klonowanie ludzkich podtypów receptora serotoniny 5-HT2 i 5-HT1C”. Komunikacja badań biochemicznych i biofizycznych . 181 (3): 1469–78. doi : 10.1016/0006-291X(91)92105-S . PMID 1722404 .
- Lappalainen J, Zhang L, Dean M, Oz M, Ozaki N, Yu DH, Virkkunen M, Waga F, Linnoila M, Goldman D (maj 1995). „Identyfikacja, ekspresja i farmakologia podstawienia Cys23-Ser23 w genie ludzkiego receptora 5-HT2c (HTR2C)” . Genomika . 27 (2): 274–9. doi : 10.1006/geno.1995.1042 . PMID 7557992 .
- Tecott LH, Sun LM, Akana SF, Strack AM, Lowenstein DH, Dallman MF, Julius D (kwiecień 1995). „Zaburzenie odżywiania i padaczka u myszy pozbawionych receptorów serotoniny 5-HT2c”. Natura . 374 (6522): 542-6. Kod Bib : 1995Natur.374..542T . doi : 10.1038/374542a0 . PMID 7700379 . S2CID 4368727 .
- Stam NJ, Vanderheyden P, van Alebeek C, Klomp J, de Boer T, van Delft AM, Olijve W (listopad 1994). „Organizacja genomowa i funkcjonalna ekspresja genu kodującego ludzki receptor serotoniny 5-HT2C”. European Journal of Pharmacology . 269 (3): 339–48. doi : 10.1016/0922-4106(94)90042-6 . PMID 7895773 .
- Xie E, Zhu L, Zhao L, Chang LS (sierpień 1996). „Ludzki receptor serotoniny 5-HT2C: kompletny cDNA, struktura genomowa i wariant alternatywnie splicing”. Genomika . 35 (3): 551–61. doi : 10.1006/geno.1996.0397 . PMID 8812491 .
- Burns CM, Chu H, Rueter SM, Hutchinson LK, Canton H, Sanders-Bush E, Emeson RB (maj 1997). „Regulacja sprzężenia białka G receptora serotoniny-2C przez edycję RNA”. Natura . 387 (6630): 303-8. Kod Bib : 1997Natur.387..303B . doi : 10.1038/387303a0 . PMID 9153397 . S2CID 4247011 .
- Brennan TJ, Seeley WW, Kilgard M, Schreiner CE, Tecott LH (sierpień 1997). „Napady wywołane dźwiękiem u myszy zmutowanych receptorem serotoniny 5-HT2c”. Genetyka przyrody . 16 (4): 387–90. doi : 10.1038/ng0897-387 . PMID 9241279 . S2CID 21333874 .
- Ullmer C, Schmuck K, Figge A, Lübbert H (marzec 1998). „Klonowanie i charakterystyka MUPP1, nowego białka domeny PDZ” . Listy FEBS . 424 (1–2): 63–8. doi : 10.1016/S0014-5793(98)00141-0 . PMID 9537516 .
- Samochowiec J, Smolka M, Winterer G, Rommelspacher H, Schmidt LG, Sander T (kwiecień 1999). „Analiza asocjacji między polimorfizmem podstawienia Cys23Ser genu ludzkiego receptora 5-HT2c a nadpobudliwością neuronalną”. American Journal of Medical Genetics . 88 (2): 126–30. doi : 10.1002/(SICI)1096-8628(19990416)88:2<126::AID-AJMG6>3.0.CO;2-M . PMID 10206230 .
- Cargill M, Altshuler D, Irlandia J, Sklar P, Ardlie K, Patil N, Shaw N, Lane CR, Lim EP, Kalyanaraman N, Nemesh J, Ziaugra L, Friedland L, Rolfe A, Warrington J, Lipshutz R, Daley GQ , Lander ES (lipiec 1999). „Charakterystyka polimorfizmów pojedynczego nukleotydu w regionach kodujących ludzkich genów”. Genetyka przyrody . 22 (3): 231–8. doi : 10.1038/10290 . PMID 10391209 . S2CID 195213008 .
- Marshall SE, Bird TG, Hart K, Welsh KI (grudzień 1999). „Ujednolicone podejście do analizy zmienności genetycznej w szlakach serotoninergicznych”. American Journal of Medical Genetics . 88 (6): 621-7. doi : 10.1002/(SICI)1096-8628(19991215)88:6<621::AID-AJMG9>3,0.CO;2-H . PMID 10581480 .
- Backstrom JR, Price RD, Reasoner DT, Sanders-Bush E (sierpień 2000). „Usunięcie motywu rozpoznawania PDZ receptora serotoninowego 5-HT2C zapobiega fosforylacji receptora i opóźnia resensytyzację odpowiedzi receptora” . Czasopismo Chemii Biologicznej . 275 (31): 23620-6. doi : 10.1074/jbc.M000922200 . PMID 10816555 .
Ten artykuł zawiera tekst z Narodowej Biblioteki Medycznej Stanów Zjednoczonych , która jest własnością publiczną .