Chlorek fosforylu - Phosphoryl chloride
|
|||
|
|
|||

|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
trichlorek fosforylu |
|||
| Inne nazwy
Tlenochlorek
fosforu Trichlorek fosforu Trichlorofosforan |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.030.030 |
||
| Numer WE | |||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
| Numer ONZ | 1810 | ||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| POCl 3 | |||
| Masa cząsteczkowa | 153,33 g/mol | ||
| Wygląd zewnętrzny | bezbarwna ciecz, opary w wilgotnym powietrzu | ||
| Zapach | ostry i stęchły | ||
| Gęstość | 1,645 g / cm 3 , ciekłe | ||
| Temperatura topnienia | 1,25 ° C (34,25 ° F; 274,40 K) | ||
| Temperatura wrzenia | 105,8 ° C (222,4 ° F; 378,9 K) | ||
| Reaguje | |||
| Rozpuszczalność | dobrze rozpuszczalny w benzenie , chloroformie , CS 2 , CCl 4 | ||
| Ciśnienie pary | 40 mmHg (27 °C) | ||
|
Współczynnik załamania ( n D )
|
1.460 | ||
| Struktura | |||
| czworościenny | |||
| 2,54 D | |||
| Termochemia | |||
|
Pojemność cieplna ( C )
|
84,35 J/mol K | ||
|
Standardowa entalpia
tworzenia (Δ f H ⦵ 298 ) |
-568,4 kJ/mol | ||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa |
Patrz: strona danych ICSC 0190 |
||
|
Klasyfikacja UE (DSD) (nieaktualna)
|
Bardzo toksyczny ( T+ ) Szkodliwy ( Xn ) Żrący ( C ) |
||
| Zwroty R (nieaktualne) | R14 , R22 , R26 , R35 , R48/23 | ||
| Zwroty S (nieaktualne) | (S1/2) , S7/8 , S26 , S36/37/39 , S45 | ||
| NFPA 704 (ognisty diament) | |||
| Dawka lub stężenie śmiertelne (LD, LC): | |||
|
LD 50 ( mediana dawki )
|
36 mg/kg (szczur, doustnie) | ||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
PEL (dopuszczalne)
|
Żaden | ||
|
REL (zalecane)
|
TWA 0,1 ppm (0,6 mg/m 3 ) ST 0,5 ppm (3 mg/m 3 ) | ||
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
NS | ||
| Związki pokrewne | |||
|
Związki pokrewne
|
Chlorek tiofosforylu Tlenobromek fosforu Trójchlorek fosforu Pięciochlorek fosforu |
||
| Strona z danymi uzupełniającymi | |||
|
Współczynnik załamania ( n ), stała dielektryczna (ε r ) itp. |
|||
|
Dane termodynamiczne |
Zachowanie fazowe ciało stałe-ciecz-gaz |
||
| UV , IR , NMR , MS | |||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Chlorek fosforylu (powszechnie nazywany tlenochlorek fosforu ) jest bezbarwną cieczą o wzorze P O Cl 3 . W wilgotnym powietrzu hydrolizuje wydzielając kwas fosforowy i opary chlorowodoru . Jest produkowany przemysłowo na dużą skalę z trójchlorku fosforu i tlenu lub pięciotlenku fosforu . Stosowany jest głównie do wytwarzania estrów fosforanowych, takich jak fosforan trikrezylu .
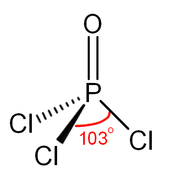
Struktura

Podobnie jak fosforan, chlorek fosforylu ma kształt czworościenny. Posiada trzy wiązania P−Cl i jedno silne wiązanie podwójne P=O, o szacowanej energii dysocjacji wiązania 533,5 kJ/mol. Na podstawie długości wiązania i elektroujemności reguła Schomakera-Stevensona sugeruje, że forma wiązania podwójnego jest dominująca, w przeciwieństwie do przypadku POF 3 . Wiązanie P=O polega na oddaniu elektronów z wolnej pary na orbitalach p tlenu do kombinacji antywiązań związanych z wiązaniami fosfor-chlor, tworząc w ten sposób wiązanie π .

Chlorek fosforylu istnieje jako obojętne POCI 3 cząsteczek w stałych , ciekłych i gazowych stanów. Jest to w przeciwieństwie do pentachlorku fosforu, który istnieje jako obojętne cząsteczki PCl 5 w stanie gazowym i ciekłym, ale przyjmuje postać jonową [PCl 4 + ][PCl 6 − ] w stanie stałym. Średnie długości wiązań w strukturze krystalicznej POCl 3 wynoszą 1,98 Å dla P–Cl i 1,46 Å dla P=O.
Właściwości fizyczne
Przy temperaturze zamarzania 1 °C i temperaturze wrzenia 106 °C zakres cieczy POCl 3 jest podobny do wody. Podobnie jak woda, POCl 3 ulega autojonizacji dzięki odwracalnemu powstawaniu POCl 2 + ,Cl − .
Właściwości chemiczne
POCl 3 reaguje z wodą dając chlorowodór i kwas fosforowy :
- O = PCl 3 + 3 H 2 O → O = P (OH) 3 + 3 HCl
Wyodrębniono związki pośrednie w konwersji, w tym chlorek pirofosforylu , P 2 O 3 Cl 4 .
Po obróbce z nadmiarem alkoholi i fenoli , POCl 3 daje estry fosforanowe :
- O=PCl 3 + 3 ROH → O=P(OR) 3 + 3 HCl
Takie reakcje często prowadzi się w obecności akceptora HCl, takiego jak pirydyna lub amina .
POCl 3 może również działać jako zasady Lewisa , tworząc addukty z różnymi Lewisa kwasy , takie jak tetrachlorek tytanu :
- Cl 3 PO + TiCl 4 → cl 3 POTiCl 4
Chlorek glinu adduktu (POCl 3 · AlCl 3 ) jest dość stabilny, a POCI 3 może być stosowany do usuwania AlCl 3 z mieszaniny reakcyjnej, na przykład na końcu reakcji Friedel-Craftsa .
POCl 3 reaguje z bromowodorem w obecności katalizatorów kwasowych Lewisa w celu wytworzenia POBr 3 .
Przygotowanie
Chlorek fosforylu można wytworzyć wieloma metodami. Chlorek fosforylu został po raz pierwszy odnotowany w 1847 roku przez francuskiego chemika Adolphe'a Wurtza w reakcji pięciochlorku fosforu z wodą.
Przez utlenianie
Sposób handlowego obejmuje utlenianie trójchlorku fosforu z tlenem :
- 2 PCl 3 + O 2 → 2 POCl 3
Alternatywna metoda polega na utlenianiu trójchlorku fosforu chloranem potasu :
Natleniania
Reakcja pięciochlorku fosforu (PCl 5 ) z pięciotlenkiem fosforu (P 4 O 10 ).
- 6 PCl 5 + P 4 O 10 → 10 POCl 3
Reakcję można uprościć przez chlorowanie mieszaniny PCl 3 i P 4 O 10 , generując PCl 5 in situ . Reakcja pentachlorku fosforu z kwasem borowym lub kwasem szczawiowym :
Inne metody
Redukcja fosforanu trójwapniowego węglem w obecności gazowego chloru :
- Ca 3 (PO 4 ) 2 + 6 C + 6 Cl 2 → 3 CaCl 2 + 6 CO + 2 POCl 3
Opisano również reakcję pięciotlenku fosforu z chlorkiem sodu :
- 2P 2 O 5 + 3 NaCl → 3 NaPO 3 + POCl 3 .
Zastosowania
W jednym z zastosowań komercyjnych chlorek fosforylu stosuje się do wytwarzania estrów fosforanowych. Fosforany triarylu, takie jak fosforan trifenylu i fosforan trikrezylu, są stosowane jako środki zmniejszające palność i plastyfikatory dla PCW . Fosforany trialkilowe, takie jak fosforan tributylu, są stosowane jako rozpuszczalniki do ekstrakcji ciecz-ciecz w przeróbce jądrowej i gdzie indziej.
W przemyśle półprzewodników POCl 3 jest wykorzystywany jako bezpieczne źródło ciekłego fosforu w procesach dyfuzji. Fosfor pełni rolę domieszki służącej do tworzenia warstw typu n na płytce krzemowej.
Jako odczynnik
W laboratorium POCl 3 jest odczynnikiem w odwodnieniach. Jeden przykład obejmuje konwersję formamidów do izonitryli (izocyjanianów); amidy pierwszorzędowe do nitryli :
- RC (O) NH 2 + POCl 3 → RCN + "Po 2 Cl" + 2 HCI
W pokrewnej reakcji, pewne amidy podstawione arylem można cyklizować stosując reakcję Bischlera-Napieralskiego .
Uważa się , że takie reakcje przebiegają przez chlorek imidoilu . W niektórych przypadkach produktem końcowym jest chlorek imidoilu. Na przykład, pirydony i pirymidony można przekształcić w pochodne chloru, takie jak 2-chloropirydyny i 2-chloropirymidyny, które są półproduktami w przemyśle farmaceutycznym.
W reakcji Vilsmeiera-Haacka , POCl 3 reaguje z amidów do wytwarzania odczynnika Vilsmeiera „”, czyli chloro iminową sól, który następnie poddaje się reakcji ze związków bogatych w elektrony aromatycznych w celu wytworzenia aromatycznych aldehydów, po obróbce wodnej.
Bibliografia
Dalsza lektura
- Podręcznik Chemii i Fizyki (wyd. 71.). Ann Arbor, MI: CRC Press. 1990.
- Stecher, Paul G. (1960). Indeks chemikaliów i leków firmy Merck (wyd. 7). Rahway: Merck & Co . OCLC 3653550 .
- Wade, LG, Jr (2005). Chemia organiczna (wyd. 6). Upper Saddle River, NJ: Pearson/Prentice Hall. P. 477.
- Walker, BJ (1972). Chemia fosforoorganiczna . Harmondsworth: Pingwin. s. 101–116.
- „CDC – Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych” .