Adamantan - Adamantane

|
|

|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Adamantane |
|
|
Systematyczna nazwa IUPAC
Tricyklo[3.3.1.1 3,7 ]dekan |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 1901173 | |
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Karta informacyjna ECHA |
100.005.457 |
| Numer WE | |
| 26963 | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 10 H 16 | |
| Masa cząsteczkowa | 136,238 g·mol -1 |
| Wygląd zewnętrzny | Proszek o barwie od białej do złamanej bieli |
| Gęstość | 1,08 g / cm 3 (20 ° C) substancję stałą |
| Temperatura topnienia | Uszczelniona rura 270 °C (518 °F; 543 K) |
| Temperatura wrzenia | Wzniosłość |
| Słabo rozpuszczalny | |
| Rozpuszczalność w innych rozpuszczalnikach | Rozpuszczalny w węglowodorach |
|
Współczynnik załamania ( n D )
|
1,568 |
| Struktura | |
| sześcienny , grupa kosmiczna Fm3m | |
| 4 | |
| 0 D | |
| Zagrożenia | |
| Główne zagrożenia | Zapalny |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Ostrzeżenie |
| H319 , H400 | |
| P264 , P273 , P280 , P305+351+338 , P337+313 , P391 , P501 | |
| Związki pokrewne | |
|
Związki pokrewne:
|
Memantyna Rymantadyna Amantadyna |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
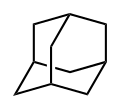
Szczawian jest organiczny związek o wzorze C 10 H 16 lub więcej opisowej (CH) 4 (CH 2 ) 6 . Cząsteczki adamantanu można opisać jako fuzję trzech pierścieni cykloheksanowych . Cząsteczka jest zarówno sztywna, jak i praktycznie pozbawiona naprężeń. Adamantane jest najbardziej stabilnym izomerem C 10 H 16 . Przestrzenny układ atomów węgla w cząsteczce adamantanu jest taki sam jak w krysztale diamentu . To podobieństwo doprowadziło do nazwy adamantan , która wywodzi się od greckiego adamantinos (odnoszącego się do stali lub diamentu ). Jest to białe ciało stałe o zapachu przypominającym kamforę . Jest to najprostszy diamentoid .
Odkrycie adamantanu w ropie naftowej w 1933 roku zapoczątkowało nową dziedzinę chemii poświęconą syntezie i właściwościom wielościennych związków organicznych. Pochodne adamantanu znalazły praktyczne zastosowanie jako leki, materiały polimerowe i termicznie stabilne smary.
Historia i synteza
W 1924 roku H. Decker zasugerował istnienie adamantanu, który nazwał dekaterpenem .
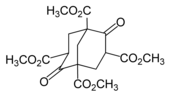
Pierwszą próbę laboratoryjną syntezy podjął w 1924 r. niemiecki chemik Hans Meerwein w reakcji formaldehydu z malonianem dietylu w obecności piperydyny . Zamiast adamantanu Meerwein otrzymał 1,3,5,7-tetrakarbometoksybicyklo[3.3.1]nonano-2,6-dion: związek ten, nazwany później estrem Meerweina, został użyty w syntezie adamantanu i jego pochodnych. D. Bottger próbował otrzymać adamantan używając jako prekursora estru Meerweina. Produkt, tricyklo-[3.3.1.1 3,7 ], nie był adamantanem, lecz pochodną.
Inni badacze próbowali zsyntetyzować adamantan przy użyciu floroglucynolu i pochodnych cykloheksanonu , ale również im się nie udało.
Adamantan został po raz pierwszy zsyntetyzowany przez Vladimira Preloga w 1941 roku z estru Meerweina. Przy wydajności 0,16% pięcioetapowy proces był niepraktyczny (uproszczony na poniższym obrazku). Metoda służy do syntezy niektórych pochodnych adamantanu.
Metoda Preloga została udoskonalona w 1956 roku. Wydajność dekarboksylacji została zwiększona przez dodanie szlaku Heinsdeckera (11%) i reakcji Hoffmana (24%), które podniosły całkowitą wydajność do 6,5%. Proces wciąż był zbyt złożony, a wygodniejszą metodę odkrył w 1957 Paul von Ragué Schleyer : dicyklopentadien najpierw uwodorniano w obecności katalizatora (np. dwutlenku platyny ), a następnie przekształcano w adamantan przy użyciu kwasu Lewisa (np. chlorku glinu). ) jako kolejny katalizator. Ta metoda zwiększyła wydajność do 30-40% i zapewniła niedrogie źródło adamantanu; w związku z tym stymulował charakteryzację adamantanu i jest nadal stosowany w praktyce laboratoryjnej. Wydajność syntezy adamantanu została później zwiększona do 60% i 98% za pomocą katalizatorów ultradźwiękowych i superkwasowych . Obecnie adamantan jest przystępnym cenowo związkiem chemicznym, którego koszt wynosi około 1 dolara za gram.
Wszystkie powyższe metody dają adamantan w postaci proszku polikrystalicznego. Stosując ten proszek można wyhodować monokryształy ze stopu, roztworu lub fazy gazowej (np. techniką Bridgmana–Stockbargera ). Wzrost w stanie stopionym daje najgorszą jakość krystaliczną z mozaikowym rozrzutem w odbiciu rentgenowskim około 1°. Najlepsze kryształy uzyskuje się z fazy ciekłej, ale wzrost jest niepraktycznie powolny – kilka miesięcy dla kryształu 5–10 mm. Wzrost z fazy gazowej jest rozsądnym kompromisem pod względem szybkości i jakości. Adamantan jest sublimowany w kwarcowej rurze umieszczonej w piecu, który jest wyposażony w kilka grzałek utrzymujących pewien gradient temperatury (około 10 °C/cm dla adamantanu) wzdłuż rury. Krystalizacja zaczyna się na jednym końcu rurki, która jest utrzymywana w pobliżu punktu zamarzania adamantanu. Powolne schładzanie probówki, przy zachowaniu gradientu temperatury, stopniowo przesuwa strefę topnienia (szybkość ~2 mm/godz.) tworząc kulkę monokryształu .
Naturalne występowanie
Adamantan został po raz pierwszy wyizolowany z ropy naftowej przez czeskich chemików S. Landę, V. Machacka i M. Mzourka. Wykorzystali destylację frakcyjną na bazie ropy naftowej. Landa i in. mógł wyprodukować tylko kilka miligramów adamantanu, ale zauważył jego wysoką temperaturę wrzenia i topnienia . Ze względu na (zakładane) podobieństwo jego budowy do diamentu, nowy związek nazwano adamantanem.
Ropa naftowa pozostaje źródłem adamantanu; zawartość waha się od 0,0001% do 0,03% w zależności od pola naftowego i jest zbyt niska dla produkcji komercyjnej.
Nafta zawiera ponad trzydzieści pochodnych adamantanu. Ich izolacja ze złożonej mieszaniny węglowodorów jest możliwa dzięki ich wysokiej temperaturze topnienia oraz zdolności do destylacji z parą wodną i tworzenia trwałych adduktów z tiomocznikiem .
Właściwości fizyczne
Czysty adamantan to bezbarwne, krystaliczne ciało stałe o charakterystycznym zapachu kamfory. Jest praktycznie nierozpuszczalny w wodzie, ale łatwo rozpuszczalny w niepolarnych rozpuszczalnikach organicznych . Adamantan ma niezwykle wysoką temperaturę topnienia jak na węglowodór . W temperaturze 270 °C jego temperatura topnienia jest znacznie wyższa niż innych węglowodorów o tej samej masie cząsteczkowej, takich jak kamfen (45 °C), limonen (-74 °C), ocimen (50 °C), terpinen (60 °C) lub twistane (164 ° C) lub linearnego C 10 H 22 węglowodór dekan (-28 ° C). Jednak adamantan powoli sublimuje nawet w temperaturze pokojowej. Adamantan można destylować z parą wodną .
Struktura
Jak wywnioskować dyfrakcji elektronów i krystalografii rentgenowskiej , molekuła T d symetrii. Długości wiązań węgiel-węgiel wynoszą 1,54 Å , prawie identyczne jak w przypadku diamentu. Odległości węgiel-wodór wynoszą 1,112 Å.
W warunkach otoczenia adamantan krystalizuje w sześciennej strukturze skoncentrowanej na twarzy ( grupa przestrzenna Fm3m, a = 9,426 ± 0,008 Å , cztery cząsteczki w komórce elementarnej ) zawierającej cząsteczki adamantanu o orientacji nieuporządkowanej. Ta struktura przekształca się w uporządkowaną, prymitywną fazę tetragonalną ( a = 6,641 Å , c = 8,875 Å ) z dwiema cząsteczkami na komórkę, po schłodzeniu do 208 K lub ciśnieniu powyżej 0,5 GPa.
To przejście fazowe jest pierwszego rzędu; towarzyszy mu anomalia w pojemności cieplnej , sprężystości i innych właściwościach. W szczególności, podczas gdy cząsteczki adamantanu swobodnie obracają się w fazie sześciennej, są zamrożone w fazie tetragonalnej; gęstość wzrasta się skokowo od 1,08 do 1,18 g / cm 3 i entropii zmienia się o znacznej wysokości 1594 J / (mol ° K).
Twardość
Stałe sprężystości adamantanu mierzono przy użyciu dużych (centymetrowych) monokryształów i ultradźwiękowej techniki echa. Główna wartość tensora sprężystości , C 11 , została wyznaczona jako 7,52, 8,20 i 6,17 GPa dla kierunków krystalicznych <110>, <111> i <100>. Dla porównania odpowiednie wartości dla diamentu krystalicznego to 1161, 1174 i 1123 GPa. Układ atomów węgla jest taki sam w adamantanie i diamencie. Jednak w adamantanowym ciele stałym cząsteczki nie tworzą sieci kowalencyjnej jak w diamencie, ale oddziałują poprzez słabe siły Van der Waalsa . Dzięki temu kryształy adamantanu są bardzo miękkie i plastyczne.
Spektroskopia
Jądrowego rezonansu magnetycznego (NMR) adamantanu składa się z dwóch źle rozdzielonych sygnałów, które odnoszą się do miejsc 1 i 2 (patrz rysunek). 1 H 13 C NMR chemiczne przesunięcia odpowiednio 1,873 i 1,756 ppm, to 28,46 i 37,85 ppm. Prostota tych widm jest zgodna z symetrią wysokocząsteczkową.
Charakterystyczne są widma masowe adamantanu i jego pochodnych. Główny pik przy m / z = 136 odpowiada C
10h+
16jon. Jego fragmentacja skutkuje słabszymi sygnałami, ponieważ m / z = 93, 80, 79, 67, 41 i 39.
Widmo absorpcji w podczerwieni z adamantanem jest stosunkowo proste, ponieważ wysokiej symetrii cząsteczki. Główne pasma absorpcji i ich przypisanie podano w tabeli:
| Częstotliwość drgań, cm −1 | Zadanie * |
|---|---|
| 444 | (CCC) |
| 638 | (CCC) |
| 798 | ν(C-C) |
| 970 | ρ (CH 2 ) ν (C = C), δ (HCC) |
| 1103 | δ(HCC) |
| 1312 | ν (C = C), ω (CH 2 ) |
| 1356 | δ (HCC), ω (CH 2 ) |
| 1458 | (HCH) |
| 2850 | ν (CH) w CH 2 grupami |
| 2910 | ν (CH) w CH 2 grupami |
| 2930 | ν (CH) w CH 2 grupami |
* Legenda odpowiadają rodzajów drgań: hemibursztynianu - odkształcenia, v - rozciąganie, p i omów - poza płaszczyzną drgań deformacyjnych CH 2 grupach.
Aktywność optyczna
Pochodne adamantanu z różnymi podstawnikami na każdym węzłowym miejscu węgla są chiralne . Taka aktywność optyczna została opisana w adamantanie w 1969 z czterema różnymi podstawnikami będącymi wodorem , bromem oraz grupą metylową i karboksylową . Wartości rotacji właściwej są małe i zwykle mieszczą się w granicach 1°.
Nomenklatura
Używając zasad systematycznej nomenklatury, adamantan nazywa się tricyklo[3.3.1.1 3,7 ]dekanem. Jednak IUPAC zaleca używanie nazwy „adamantan”.
Adamantan cząsteczka składa się tylko z węgla i wodoru i ma T d symetrii. Dlatego jego 16 atomów wodoru i 10 atomów węgla można opisać tylko dwoma miejscami, które są oznaczone na rysunku jako 1 (4 równoważne miejsca) i 2 (6 równoważnych miejsc).
Krewni strukturalne adamantan są noradamantane i homoadamantane , które odpowiednio zawierają jeden mniej i jeszcze jedno CH 2 łącza niż adamantan.
Właściwości chemiczne
Kationy adamantanowe
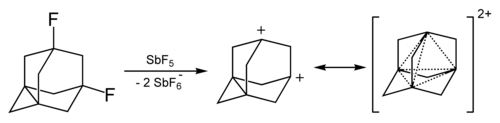
Adamantan kation może być wytwarzany przez potraktowanie 1-fluoro-adamantan z SbF 5 . Jego stabilność jest stosunkowo wysoka.
Dication 1,3-didehydroadamantane otrzymano w roztworach superkwasów . Ma również podwyższoną stabilność dzięki zjawisku zwanemu „trójwymiarową aromatycznością” lub homoaromatycznością . To czterocentrowe wiązanie dwuelektronowe obejmuje jedną parę elektronów zdelokalizowanych pomiędzy czterema atomami przyczółkowymi.
Reakcje
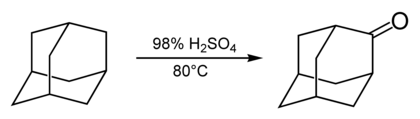
Większość reakcji adamantanu zachodzi za pośrednictwem 3-koordynowanych miejsc węglowych. Biorą udział w reakcji adamantanu ze stężonym kwasem siarkowym, w wyniku której powstaje adamantanon .
Grupa karbonylowa adamantanonu umożliwia dalsze reakcje za pośrednictwem miejsca mostkowania. Na przykład, adamantanon jest związkiem wyjściowym do otrzymywania takich pochodnych adamantanu jak 2-adamantanokarbonitryl i 2-metyloadamantan.
Bromacja
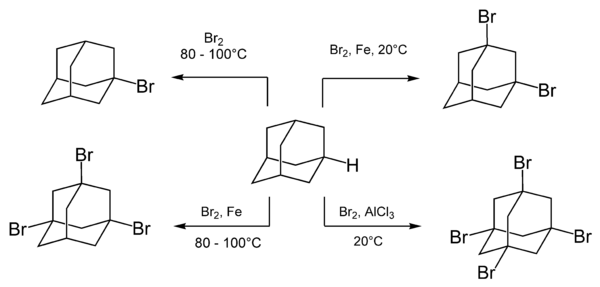
Adamantan łatwo reaguje z różnymi środkami bromującymi, w tym z cząsteczkowym bromem . Skład i stosunek produktów reakcji zależą od warunków reakcji, a zwłaszcza obecności i rodzaju katalizatorów .
Gotowanie adamantanu z bromem daje monopodstawiony adamantan, 1-bromadamantan. Wielokrotne podstawienie bromem uzyskuje się przez dodanie katalizatora kwasu Lewisa .
Szybkość bromowania zwiększa się po dodaniu kwasów Lewisa i pozostaje niezmieniona przez napromieniowanie lub dodanie wolnych rodników. Wskazuje to, że reakcja zachodzi poprzez mechanizm jonowy.
Fluorowanie
Pierwsze fluorowania adamantanu przeprowadzono stosując jako związki wyjściowe 1-hydroksyadamantan i 1-aminoadamantan. Później uzyskano fluorowanie, zaczynając od samego adamantanu. We wszystkich tych przypadkach reakcja przebiegała przez tworzenie kationu adamantanu, który następnie oddziaływał z fluorowanymi nukleofilami. Donoszono również o fluorowaniu adamantanu gazowym fluorem .
Karboksylacja
Karboksylację adamantanu po raz pierwszy opisano w 1960 roku, stosując kwas mrówkowy jako środek karboksylujący i tetrachlorek węgla jako rozpuszczalnik.
tert -butanol ( t- BuOH) i kwas siarkowy dodano w celu wytworzenia kationu adamantanu; kation był następnie karboksylowany przez tlenek węgla wytworzony in situ w interakcji między kwasem mrówkowym i siarkowym . Frakcja karboksylowanego adamantanu wynosiła 55-60%.
Utlenianie
1-Hydroksyadamantan łatwo powstaje przez hydrolizę 1-bromadamantanu w wodnym roztworze acetonu . Może być również wytwarzany przez ozonowanie adamantanu: Utlenianie alkoholu daje adamantanon .
Inni
Adamantan wchodzi w interakcję z benzenem w obecności kwasów Lewisa, powodując reakcję Friedla-Craftsa . Pochodne adamantanu podstawione arylem można łatwo otrzymać wychodząc z 1-hydroksyadamantanu. W szczególności reakcja z anizolem przebiega w normalnych warunkach i nie wymaga katalizatora.
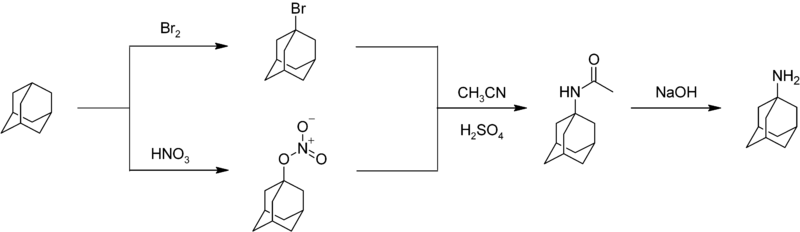
Azotowanie adamantanu jest trudną reakcją charakteryzującą się umiarkowanymi wydajnościami. Lek amantadynę podstawiony azotem można wytworzyć w reakcji adamantanu z bromem lub kwasem azotowym z wytworzeniem bromku lub nitroestru w pozycji 1 . Reakcja każdego związku z acetonitrylem daje acetamid, który hydrolizuje dając 1-adamantyloaminę:
Zastosowania
Sam adamantan ma niewiele zastosowań, ponieważ jest jedynie węglowodorem niefunkcjonalizowanym . Jest stosowany w niektórych suchych maseczkach do trawienia i preparatach polimerowych .
W spektroskopii NMR ciała stałego adamantan jest powszechnym standardem odniesienia przesunięcia chemicznego .
W laserach barwnikowych adamantan może być stosowany w celu przedłużenia żywotności ośrodka wzmacniającego; nie może być fotojonizowany w atmosferze, ponieważ jego pasma absorpcyjne leżą w obszarze widma próżniowo-ultrafioletowego . Energie fotojonizacji zostały określone zarówno dla adamantanu, jak i kilku większych diamentoidów .
W medycynie
Wszystkie znane dotychczas zastosowania medyczne dotyczą nie czystego adamantanu, ale jego pochodnych. Pierwszą pochodną adamantanu zastosowaną jako lek była amantadyna – najpierw (1967) jako lek przeciwwirusowy przeciwko różnym szczepom grypy, a następnie do leczenia choroby Parkinsona . Inne leki wśród pochodnych adamantanu obejmują adapalen , adaprominę , bromantan , karmantadynę , chlodantan , dopamantynę , memantynę , rymantadynę , saksagliptynę , tromantadynę i wildagliptynę . Polimery adamantanu zostały opatentowane jako środki przeciwwirusowe przeciwko HIV .
Szczepy wirusa grypy rozwinęły lekooporność na amantadynę i rymantadynę, które od 2016 r. nie są skuteczne wobec powszechnie występujących szczepów.
W markowych lekach
Adamantan został niedawno zidentyfikowany jako kluczowa podjednostka strukturalna w kilku syntetycznych lekach kannabinoidowych , a mianowicie AB-001 i SDB-001 .
Paliwo do statków kosmicznych
Adamantane jest atrakcyjnym kandydatem na paliwo w silnikach Halla, ponieważ łatwo się jonizuje, może być przechowywany w postaci stałej, a nie w zbiorniku o wysokim ciśnieniu i jest stosunkowo nietoksyczny.
Potencjalne zastosowania technologiczne
Niektóre pochodne alkilowe adamantanu są stosowane jako płyn roboczy w układach hydraulicznych . Polimery na bazie adamantanu mogą znaleźć zastosowanie w powłokach ekranów dotykowych , a adamantan i jego homologi mogą zostać wykorzystane w nanotechnologii . Na przykład, miękka struktura przypominająca klatkę adamantanu pozwala na wprowadzenie cząsteczek gościa, które mogą zostać uwolnione do wnętrza ludzkiego ciała po rozbiciu matrycy. Adamantan można wykorzystać jako molekularne elementy budulcowe do samodzielnego składania kryształów molekularnych.
Analogi Adamantanu
Wiele cząsteczek i jonów przyjmuje struktury klatkowe podobne do adamantanu. Należą do nich trójtlenek fosforu P 4 O 6 , trójtlenek arsenu As 4 O 6 , pięciotlenek fosforu P 4 O 10 = (PO) 4 O 6 , pięciosiarczek fosforu P 4 S 10 = (PS) 4 S 6 , oraz heksametylenotetramina C 6 N 4 H 12 = N 4 (CH 2 ) 6 . Szczególnie znana jest tetrametylenodisulfotetramina , często skracana do „tetramina”, rodentycyd zakazany w większości krajów ze względu na skrajną toksyczność dla ludzi. Analog krzemu adamantanowe, sila-adamantanu, zsyntetyzowano 2005 arsenicyna a jest naturalnie występującym arsenoorganiczne analog odizolowane od Nowy Kaledońskiego morskich gąbka Echinochalina bargibanti i jest pierwszym znanym polyarsenic związek organiczny.
Łączenie klatek adamantanowych daje wyższe diamentoidy , takie jak diamantan (C 14 H 20 – dwie skondensowane klatki adamantanowe), triamantan (C 18 H 24 ), tetramantan (C 22 H 28 ), pentamantan (C 26 H 32 ), heksamantan (C 26 H 30 ), itp. Ich synteza jest podobna do syntezy adamantanu i podobnie jak adamantan można je również ekstrahować z ropy naftowej, chociaż z jeszcze znacznie mniejszymi wydajnościami.